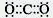题目内容
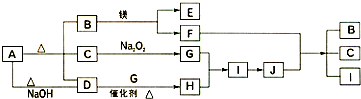
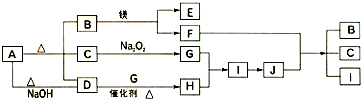
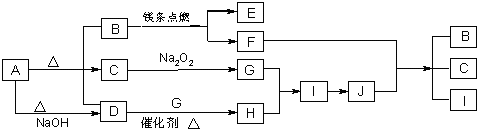
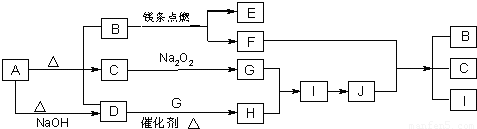
如图中A~J分别代表相关反应中的一种物质,已知A分解得到等物质的量的B、C、D,已知B、D为常温下气态化合物,C为常温下液态化合物,图中有部分生成物未标出.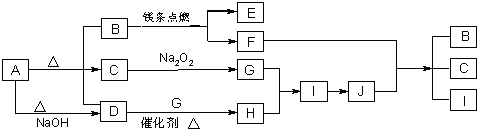
请填写以下空白:
(1)A的化学式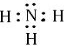
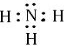 .
.
(2)写出下列反应的化学方程式:
D+G→H
F+J→B+C+I
(3)0.3mol I与足量C反应转移电子的物质的量为
(4)容积为10mL的试管中充满I和G的混合气体,倒立于盛水的水槽中,水全部充满试管,则原混合气体中I的体积为

请填写以下空白:
(1)A的化学式
NH4HCO3
NH4HCO3
D的电子式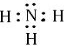
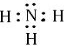
(2)写出下列反应的化学方程式:
D+G→H
4NH3+5O2
4NO+6H2O
| ||
| 高温高压 |
4NH3+5O2
4NO+6H2O
.
| ||
| 高温高压 |
F+J→B+C+I
C+4HNO3(浓)
CO2↑+4NO2↑+2H2O
| ||
C+4HNO3(浓)
CO2↑+4NO2↑+2H2O
.
| ||
(3)0.3mol I与足量C反应转移电子的物质的量为
0.2
0.2
mol.(4)容积为10mL的试管中充满I和G的混合气体,倒立于盛水的水槽中,水全部充满试管,则原混合气体中I的体积为
8
8
mL.分析:A受热能分解,分解得到等物质的量的B、C、D,且A与碱反应生成气体D,B、D为常温下气态化合物,C为常温下液态化合物,C为水,则A为NH4HCO3,B能与镁反应,则B为CO2,E为MgO,F为C,结合D为NH3,水与过氧化钠反应生成G,G为O2,D与G反应生成H,H为NO,I为NO2,J为HNO3,再结合F与J反应生成B、C、I,符合上述转化,然后结合物质的性质及题目要求来解答.
解答:解:A受热能分解,分解得到等物质的量的B、C、D,且A与碱反应生成气体D,B、D为常温下气态化合物,C为常温下液态化合物,C为水,则A为NH4HCO3,B能与镁反应,则B为CO2,E为MgO,F为C,结合D为NH3,水与过氧化钠反应生成G,G为O2,D与G反应生成H,H为NO,I为NO2,J为HNO3,再结合F与J反应生成B、C、I,符合上述转化,
(1)由上述分析可知A为NH4HCO3,D为NH3,其电子式为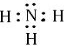 ,故答案为:NH4HCO3;
,故答案为:NH4HCO3;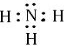 ;
;
(2)D+G→H的反应为4NH3+5O2
4NO+6H2O,F+J→B+C+I的反应为C+4HNO3(浓)
CO2↑+4NO2↑+2H2O,
故答案为:4NH3+5O2
4NO+6H2O;C+4HNO3(浓)
CO2↑+4NO2↑+2H2O;
(3)由3NO2+H2O═2HNO3+NO,则0.3molNO2与足量C反应,0.1mol作氧化剂,转移电子的物质的量为0.1mol×(4-2)=0.2mol,故答案为:0.2;
(4)由4NO2+O2+2H2O═4HNO3,倒立于盛水的水槽中,水全部充满试管,则原混合气体中I占
,其体积为10mL×
=8mL,故答案为:8.
(1)由上述分析可知A为NH4HCO3,D为NH3,其电子式为
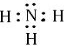 ,故答案为:NH4HCO3;
,故答案为:NH4HCO3;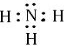 ;
;(2)D+G→H的反应为4NH3+5O2
| ||
| 高温高压 |
| ||
故答案为:4NH3+5O2
| ||
| 高温高压 |
| ||
(3)由3NO2+H2O═2HNO3+NO,则0.3molNO2与足量C反应,0.1mol作氧化剂,转移电子的物质的量为0.1mol×(4-2)=0.2mol,故答案为:0.2;
(4)由4NO2+O2+2H2O═4HNO3,倒立于盛水的水槽中,水全部充满试管,则原混合气体中I占
| 4 |
| 5 |
| 4 |
| 5 |
点评:本题考查无机物的推断,利用物质的转化推断出各物质是解答本题的关键,C及A为解答本题的突破口,题目难度中等.

练习册系列答案
相关题目