题目内容
设NA代表阿伏加德罗常数,下列说法正确的是
- A.23g金属钠变为钠离子时得到的电子数为NA
- B.标准状况下,18g水所含的中子数目为10NA
- C.标准状况下,22.4L氦气所含的原子数目为NA
- D.常温常压下,2.8gN2和CO的混合气体所含原子数为0.2NA
CD
分析:A、1个钠原子失去1个电子形成钠离子;
B、1个水分子含有8个中子;
C、稀有气体是单原子分子;
D、N2和CO的摩尔质量相同为28g/mol,所以平均摩尔质量为28g/mol,每个分子都含2个原子,先计算混合气体物质的量,根据N=nNA计算.
解答:A、金属钠变为钠离子时失去电子,不是得到电子,故A错误;
B、18g水所含的中子数目为 ×8×NAmol-1=8NA,故B错误;
×8×NAmol-1=8NA,故B错误;
C、稀有气体是单原子分子,标准状况下,22.4L氦气所含的原子数目为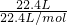 ×NAmol-1=NA,故C正确;
×NAmol-1=NA,故C正确;
D、2.8gN2和CO的混合气体的物质的量为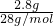 =0.1mol,每个分子都含2个原子,所含原子数为0.1mol×2×NAmol-1=0.2NA,故D正确;
=0.1mol,每个分子都含2个原子,所含原子数为0.1mol×2×NAmol-1=0.2NA,故D正确;
故选CD.
点评:本题考查常用化学计量数的有关计算,难度较小,注意稀有气体是单原子分子,D中摩尔质量相同.
分析:A、1个钠原子失去1个电子形成钠离子;
B、1个水分子含有8个中子;
C、稀有气体是单原子分子;
D、N2和CO的摩尔质量相同为28g/mol,所以平均摩尔质量为28g/mol,每个分子都含2个原子,先计算混合气体物质的量,根据N=nNA计算.
解答:A、金属钠变为钠离子时失去电子,不是得到电子,故A错误;
B、18g水所含的中子数目为
 ×8×NAmol-1=8NA,故B错误;
×8×NAmol-1=8NA,故B错误;C、稀有气体是单原子分子,标准状况下,22.4L氦气所含的原子数目为
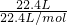 ×NAmol-1=NA,故C正确;
×NAmol-1=NA,故C正确;D、2.8gN2和CO的混合气体的物质的量为
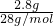 =0.1mol,每个分子都含2个原子,所含原子数为0.1mol×2×NAmol-1=0.2NA,故D正确;
=0.1mol,每个分子都含2个原子,所含原子数为0.1mol×2×NAmol-1=0.2NA,故D正确;故选CD.
点评:本题考查常用化学计量数的有关计算,难度较小,注意稀有气体是单原子分子,D中摩尔质量相同.

练习册系列答案
相关题目