��Ŀ����
��2013?Ϋ��ģ�⣩[��ѧ--���ʽṹ������]
����aX��bY��cZ����Ԫ�أ���֪���ٸ�ԭ������a��b��c��С��20����a+b+c=25����Ԫ�� Y��ԭ����Χ���ӹ���Ϊns2npn+2����X��Y�ڲ�ͬ�����¿��γ�X2Y��X2Y2���ֻ����Y��Z�ڲ�ͬ�����¿��γ�ZY��ZY2���ֻ������Z���������Է���������Z�Ȼ������Է�������֮��Ϊ38��77�����Ͽ���֪
��1��Y
��2��X2Y2��
��3��Z��������Ȼ���ķ��ӿռ乹�ͷֱ���
����aX��bY��cZ����Ԫ�أ���֪���ٸ�ԭ������a��b��c��С��20����a+b+c=25����Ԫ�� Y��ԭ����Χ���ӹ���Ϊns2npn+2����X��Y�ڲ�ͬ�����¿��γ�X2Y��X2Y2���ֻ����Y��Z�ڲ�ͬ�����¿��γ�ZY��ZY2���ֻ������Z���������Է���������Z�Ȼ������Է�������֮��Ϊ38��77�����Ͽ���֪
��1��Y
O
O
��ZC
C
����дԪ�ط��ţ���2��X2Y2��
����
����
���壨������ͣ����þ��������������������Ӽ����Ǽ��Լ�
���Ӽ����Ǽ��Լ�
����3��Z��������Ȼ���ķ��ӿռ乹�ͷֱ���
ֱ����
ֱ����
������������
����������
������Zԭ�ӷֱ���sp
sp
��sp3
sp3
�ӻ�����ɼ���������Ԫ��Y��ԭ�Ӽ۵����Ų�Ϊns2npn+2����Y�ļ۵����Ų�����Ϊ2s22p4��3s23p5��ΪOԪ�ػ�ClԪ�أ�
X��Y�ڲ�ͬ�����¿��γ�X2Y��X2Y2���ֹ�̬�����ӦΪNa2O��Na2O2������XΪNaԪ�أ�YΪOԪ�أ�������ԭ������֮��Ϊ25����Z��ԭ������Ϊ25-11-8=6��ӦΪCԪ�أ�O��C�ڲ�ͬ�����¿��γ�CO��CO2������̬�����Ԫ��C��������Ԫ��C���Ȼ�������¾�ΪҺ̬���ֱ�ΪCS2��CCl4���Ҷ��ߵ���Է�������֮��Ϊ76��154=38��77����֤���ϣ����Ԫ�ض�Ӧ�ĵ��ʡ�����������ʽ����⣮
X��Y�ڲ�ͬ�����¿��γ�X2Y��X2Y2���ֹ�̬�����ӦΪNa2O��Na2O2������XΪNaԪ�أ�YΪOԪ�أ�������ԭ������֮��Ϊ25����Z��ԭ������Ϊ25-11-8=6��ӦΪCԪ�أ�O��C�ڲ�ͬ�����¿��γ�CO��CO2������̬�����Ԫ��C��������Ԫ��C���Ȼ�������¾�ΪҺ̬���ֱ�ΪCS2��CCl4���Ҷ��ߵ���Է�������֮��Ϊ76��154=38��77����֤���ϣ����Ԫ�ض�Ӧ�ĵ��ʡ�����������ʽ����⣮
����⣺Ԫ��Y��ԭ�Ӽ۵����Ų�Ϊns2npn+2����Y�ļ۵����Ų�����Ϊ2s22p4��3s23p5��ΪOԪ�ػ�ClԪ�أ�
X��Y�ڲ�ͬ�����¿��γ�X2Y��X2Y2���ֹ�̬�����ӦΪNa2O��Na2O2������XΪNaԪ�أ�YΪOԪ�أ�������ԭ������֮��Ϊ25����Z��ԭ������Ϊ25-11-8=6��ӦΪCԪ�أ�O��C�ڲ�ͬ�����¿��γ�CO��CO2������̬�����Ԫ��C��������Ԫ��C���Ȼ�������¾�ΪҺ̬���ֱ�ΪCS2��CCl4���Ҷ��ߵ���Է�������֮��Ϊ76��154=38��77����֤���ϣ�
��1��������������֪��YΪOԪ�أ�ZΪCԪ�أ��ʴ�Ϊ��O��C��
��2��X2Y2��Na2O2��������������������ӹ��ɣ��������ӻ���������������������֮���γ����Ӽ�����������������ԭ��֮���γɷǼ��Լ����ʴ�Ϊ�����ӣ����Ӽ����Ǽ��Լ���
��3��CS2��CO2�ļ۵�����Ŀ��ȣ�Ϊ�ȵ����壬�ṹ���ƣ�Ϊֱ���ͷ��ӣ�CCl4�����Ľṹ���ƣ�Ϊ�������壻
CS2�ĽṹʽΪS=C=S������2���Ҽ���2���м���Cԭ��û�й¶Ե��ӣ��ӻ������Ϊ2����ȡsp�ӻ���CCl4�У�Cԭ����4��Clԭ���γ�4�����ۼ���ӦΪsp3�ӻ���
�ʴ�Ϊ��ֱ���͡��ȵ����壻sp��sp3��
X��Y�ڲ�ͬ�����¿��γ�X2Y��X2Y2���ֹ�̬�����ӦΪNa2O��Na2O2������XΪNaԪ�أ�YΪOԪ�أ�������ԭ������֮��Ϊ25����Z��ԭ������Ϊ25-11-8=6��ӦΪCԪ�أ�O��C�ڲ�ͬ�����¿��γ�CO��CO2������̬�����Ԫ��C��������Ԫ��C���Ȼ�������¾�ΪҺ̬���ֱ�ΪCS2��CCl4���Ҷ��ߵ���Է�������֮��Ϊ76��154=38��77����֤���ϣ�
��1��������������֪��YΪOԪ�أ�ZΪCԪ�أ��ʴ�Ϊ��O��C��
��2��X2Y2��Na2O2��������������������ӹ��ɣ��������ӻ���������������������֮���γ����Ӽ�����������������ԭ��֮���γɷǼ��Լ����ʴ�Ϊ�����ӣ����Ӽ����Ǽ��Լ���
��3��CS2��CO2�ļ۵�����Ŀ��ȣ�Ϊ�ȵ����壬�ṹ���ƣ�Ϊֱ���ͷ��ӣ�CCl4�����Ľṹ���ƣ�Ϊ�������壻
CS2�ĽṹʽΪS=C=S������2���Ҽ���2���м���Cԭ��û�й¶Ե��ӣ��ӻ������Ϊ2����ȡsp�ӻ���CCl4�У�Cԭ����4��Clԭ���γ�4�����ۼ���ӦΪsp3�ӻ���
�ʴ�Ϊ��ֱ���͡��ȵ����壻sp��sp3��
���������⿼��ṹ����λ�ù�ϵ������ṹ�뻯ѧ�����ӻ���������ӽṹ�ȣ��ѶȲ���ע������Ԫ�ػ�������ص㣬�Ƚ��в²�����֤�ƶ�Ԫ�أ�

��ϰ��ϵ�д�
 ��������״Ԫ��ϵ�д�
��������״Ԫ��ϵ�д� �ƸԿ�����ҵ��ϵ�д�
�ƸԿ�����ҵ��ϵ�д� ��Ԫ����ĩ��ϰ�ȷ��ϵ�д�
��Ԫ����ĩ��ϰ�ȷ��ϵ�д�
�����Ŀ
 ��2013?Ϋ��ģ�⣩��ͼ������̼�����ָ������Ϣʱ����������Ҫ���٣��Ӷ�����̼�ر��Ƕ�����̼���ŷţ�������Ϊ�����ڵ�̼������ǣ�������
��2013?Ϋ��ģ�⣩��ͼ������̼�����ָ������Ϣʱ����������Ҫ���٣��Ӷ�����̼�ر��Ƕ�����̼���ŷţ�������Ϊ�����ڵ�̼������ǣ�������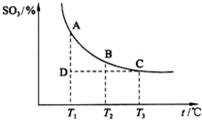 ��2013?Ϋ��ģ�⣩��ͼ���о�̼�������������������ʶԻ��������ͻ�����������Ҫ���壮
��2013?Ϋ��ģ�⣩��ͼ���о�̼�������������������ʶԻ��������ͻ�����������Ҫ���壮