题目内容
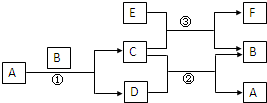
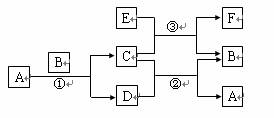
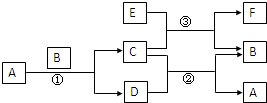 右图中所涉及的A、B、C、D、E、F和G都是中学化学教材中常见的物质.E为铝;B、D为单质,其余为化合物;反应①②③均在高温下进行且均为置换反应;A在常温下为液态,C有磁性,E、F既能溶于NaOH又能溶于HCl.
右图中所涉及的A、B、C、D、E、F和G都是中学化学教材中常见的物质.E为铝;B、D为单质,其余为化合物;反应①②③均在高温下进行且均为置换反应;A在常温下为液态,C有磁性,E、F既能溶于NaOH又能溶于HCl.(1)写出反应①的化学方程式
3Fe+4H2O
Fe3O4+4H2
| ||
3Fe+4H2O
Fe3O4+4H2
;
| ||
(2)写出E与NaOH溶液反应的离子方程式
2Al+2OH-+2H2O═2AlO2-+3H2↑
2Al+2OH-+2H2O═2AlO2-+3H2↑
;(3)用离子方程式表示F既能溶于NaOH又能溶于HCl的原因
Al2O3+2OH-=2AlO2-+H2O
Al2O3+2OH-=2AlO2-+H2O
、Al2O3+6H+=2Al3++3H2O
Al2O3+6H+=2Al3++3H2O
;(4)已知:C、E的混合物在工业上可用于钢轨焊接,请尝试写出反应③的化学方程式:
3Fe3O4+8Al
4Al2O3+9Fe
| ||
3Fe3O4+8Al
4Al2O3+9Fe
.
| ||
分析:由题意A在常温下为液态,C有磁性,可以知道A为H2O,C为Fe3O4,则B为Fe,D为H2,F既能溶于NaOH又能溶于HCl,说明F具有两性,可以联想到Al的化合物,而C又是Fe3O4,因此可以知道③为铝热反应,则E为Al,F为Al2O3,结合对应物质的性质以及题目要求可解答该题.
解答:解:由题意A在常温下为液态,C有磁性,可以知道A为H2O,C为Fe3O4,则B为Fe,D为H2,F既能溶于NaOH又能溶于HCl,说明F具有两性,可以联想到Al的化合物,而C又是Fe3O4,因此可以知道③为铝热反应,则E为Al,F为Al2O3,
(1)反应①的化学方程式为3Fe+4H2O
Fe3O4+4H2,故答案为:3Fe+4H2O
Fe3O4+4H2;
(2)E为Al,可与NaOH反应,反应的离子方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑;
(3)Al2O3具有两性,既能溶于NaOH又能溶于HCl,反应的离子方程式分别为Al2O3+2OH-=2AlO2-+H2O、Al2O3+6H+=2Al3++3H2O,
故答案为:Al2O3+2OH-=2AlO2-+H2O;Al2O3+6H+=2Al3++3H2O;
(4)③为铝热反应,反应的化学方程式为3Fe3O4+8Al
4Al2O3+9Fe,故答案为:3Fe3O4+8Al
4Al2O3+9Fe.
(1)反应①的化学方程式为3Fe+4H2O
| ||
| ||
(2)E为Al,可与NaOH反应,反应的离子方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑;
(3)Al2O3具有两性,既能溶于NaOH又能溶于HCl,反应的离子方程式分别为Al2O3+2OH-=2AlO2-+H2O、Al2O3+6H+=2Al3++3H2O,
故答案为:Al2O3+2OH-=2AlO2-+H2O;Al2O3+6H+=2Al3++3H2O;
(4)③为铝热反应,反应的化学方程式为3Fe3O4+8Al
| ||
| ||
点评:本题考查无机物的推断,该题的题眼在于A在常温下为液态,C有磁性,则可以判断为铁与高温水蒸气反应,这类推断题关键找到突破点,然后依次推断,题目难度不大.

练习册系列答案
相关题目
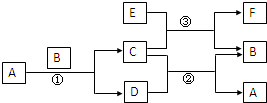 右图中所涉及的A、B、C、D、E、F和G都是中学化学教材中常见的物质.E为铝;B、D为单质,其余为化合物;反应①②③均在高温下进行且均为置换反应;A在常温下为液态,C有磁性,E、F既能溶于NaOH又能溶于HCl.
右图中所涉及的A、B、C、D、E、F和G都是中学化学教材中常见的物质.E为铝;B、D为单质,其余为化合物;反应①②③均在高温下进行且均为置换反应;A在常温下为液态,C有磁性,E、F既能溶于NaOH又能溶于HCl.