题目内容
【题目】高炉煤气为炼铁过程中产生的副产品,主要成分为CO、CO2、N2等,其中CO含量约占25%左右。
(1)研究表明,由CO可以直接合成多种化工产品,如生产甲醇。
已知:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1453kJ·mol-1
2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ·mol-1
CO(g)+2H2(g)=CH3OH(l)△H=-128.1kJ·mol-1。则CO(g)燃烧热为__________kJ·mol-1。
(2)人体中肌红蛋白(Mb)与血红蛋白(Hb)的主要功能为运输氧气与二氧化碳。肌红蛋白(Mb)可以与小分子X(如氧气或一氧化碳)结合,反应方程式为:Mb(aq)+X(g)![]() MbX(aq)
MbX(aq)
①通常用p表示分子X的压力,p0表示标准状态大气压,若X分子的平衡浓度为p/p0,写出上述反应的平衡常数表达式:K=__________.请用p/p0及K表示吸附小分子的肌红蛋白(MbX)占总肌红蛋白的比例__________。
②在常温下,肌红蛋白与CO结合反应的平衡常数K(CO)远大于与O2结合的平衡常数K(O2),下图最能代表结合率(f)与此两种气体压力(p)的关系的是____________
③人体中的血红蛋白(Hb)同样能吸附O2、CO2和H+,相关反应方程式及其化学平衡常数分别是:
Ⅰ.Hb(aq)+H+(aq)![]() HbH+(aq);K1
HbH+(aq);K1
Ⅱ.HbH+(aq)+O2(g)![]() HbHO2(aq)+H+;K2
HbHO2(aq)+H+;K2
Ⅲ.Hb(aq)+O2(g)![]() HbO2(aq)K3
HbO2(aq)K3
Ⅳ.HbO2(aq)+H+(aq)+CO2(g)![]() Hb(H+)CO2(aq)+O2(g);△H4
Hb(H+)CO2(aq)+O2(g);△H4
则K3=__________(用K1、K2表示),若低温下反应Ⅳ能自发进行,则该反应△H____0,△S__0(填“>”“<”或“=”)
(3)CO2的处理方法有多种,将少量CO2气体通入石灰乳中充分反应,达到平衡后,测得溶液中c(OH-)=cmol/L,则c(CO32-)=_____mol/L(用含a、b、c的代数式表示)。(已知Kap(CaCO3)=a,Kap[Ca(OH)2]=b)
【答案】 283 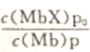
![]() C K1·K2 < < ac2/b
C K1·K2 < < ac2/b
【解析】(1)根据盖斯定律由③-②+①×![]() 可得CO气体的燃烧的热化学方程式为:CO(g)+
可得CO气体的燃烧的热化学方程式为:CO(g)+ ![]() O2(g)=CO2(g) △H=△H3-△H2+
O2(g)=CO2(g) △H=△H3-△H2+![]() △H1=+128.1kJ·mol-1-(-571.6kJ·mol-1)+(-1453kJ·mol-1) ×
△H1=+128.1kJ·mol-1-(-571.6kJ·mol-1)+(-1453kJ·mol-1) ×![]() =+283 kJ·mol-1;
=+283 kJ·mol-1;
(2)①Mb(aq)+X(g) ![]() MbX(aq)的化学平衡常数K=
MbX(aq)的化学平衡常数K= ;吸附小分子的肌红蛋白(MbX)的个数等于生成的MbX个数,由K=
;吸附小分子的肌红蛋白(MbX)的个数等于生成的MbX个数,由K=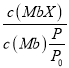 可得
可得![]() =
=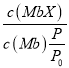 ,吸附小分子肌红蛋白(MbX)占总肌红蛋白的比例等于
,吸附小分子肌红蛋白(MbX)占总肌红蛋白的比例等于![]() =
=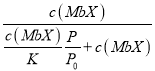 =
=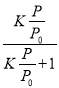 =
=![]() ;②对于Mb(aq)+X(g)
;②对于Mb(aq)+X(g) ![]() MbX(aq),增大压强,平衡正向移动,因此无论是CO还是O2,随着压强的增大,结合率(f)都是逐渐增大。在常温下,肌红蛋白与CO结合反应的平衡常数K(CO)远大于与O2结合的平衡常数K(O2),说明肌红蛋白与CO的结合能力比其与O2的结合能力强,所以相同压强条件下,肌红蛋白与CO的结合率(f)更大,因此C图象符合,答案选C;③根据盖斯定律由①+②可得反应:Hb(aq)+O2(g)
MbX(aq),增大压强,平衡正向移动,因此无论是CO还是O2,随着压强的增大,结合率(f)都是逐渐增大。在常温下,肌红蛋白与CO结合反应的平衡常数K(CO)远大于与O2结合的平衡常数K(O2),说明肌红蛋白与CO的结合能力比其与O2的结合能力强,所以相同压强条件下,肌红蛋白与CO的结合率(f)更大,因此C图象符合,答案选C;③根据盖斯定律由①+②可得反应:Hb(aq)+O2(g)![]() HbO2(aq)△H=△H1+△H2 K=K1·K2;反应Hb(aq)+O2(g)
HbO2(aq)△H=△H1+△H2 K=K1·K2;反应Hb(aq)+O2(g)![]() HbO2(aq),△S<0,由△G=△H3-T△S<0自发可知,低温下反应能自发进行,说明△H3 <0;(3)将少量CO2气体通入石灰乳中充分反应,达到平衡后发生的反应为:Ca2++CO32-
HbO2(aq),△S<0,由△G=△H3-T△S<0自发可知,低温下反应能自发进行,说明△H3 <0;(3)将少量CO2气体通入石灰乳中充分反应,达到平衡后发生的反应为:Ca2++CO32-![]() CaCO3+2OH-,平衡常数K=
CaCO3+2OH-,平衡常数K=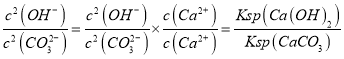 ,达到平衡后,测得溶液c(OH-)=cmol/L,则c(CO32-)=
,达到平衡后,测得溶液c(OH-)=cmol/L,则c(CO32-)= ![]() 。
。