题目内容
【题目】MnO2是一种重要的无机功能材料,粗MnO2的提纯是工业生产的重要环节.某研究性学习小组设计了将粗MnO2(含有较多的MnO和MnCO3)样品转化为纯MnO2实验,其流程如下
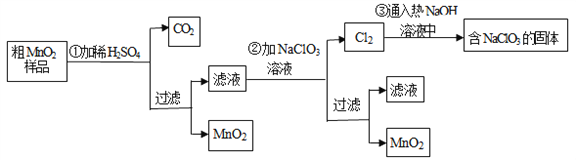
(1)第①步加稀H2SO4时,粗MnO2样品中的_____________(写化学式)转化为可溶性物质.
(2)第②步反应的离子方程式:_______________________
(3)流程中得到MnO2固体操作必需的玻璃仪器有玻璃棒、烧杯、_______________。
(4)已知第③步蒸发得到的固体中有NaClO3和NaOH,则一定还有含有_________(写化学式).其中用到Cl2的实验室制法的反应离子方程式:_______________________。
(5)若粗MnO2样品的质量为50.76g,第①步反应后,经过滤得到34.8gMnO2,并收集到0.896LCO2(标准状况下),则在第②步反应中至少需要____________ gNaClO3.[M (NaClO3)=106.5]
(6)第①步酸溶产生的CO2与NH3反应可合成化肥尿素[化学式为CO(NH2)2]。己知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s); ΔH=-159.5kJ·mol-1
②NH2CO2NH4(s)=CONH2)2(s)+H2O(g); ΔH=+116.5kJ·mol-1
③H2O(l)=H2O(g) ΔH=+44.0kJ·mol-1
写出CO2与NH3合成尿素和液态水的热化学反应方程式______________。
【答案】MnO、MnCO32ClO3-+4H2O+5Mn2+=5MnO2↓+Cl2↑+8H+漏斗NaCl4H++ MnO2+2Cl-![]() Cl2↑+Mn2++2H2O8.522NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l); ΔH=–87.0kJ·mol-1
Cl2↑+Mn2++2H2O8.522NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l); ΔH=–87.0kJ·mol-1
【解析】
试题分析:由制备流程可知,MnO2不溶于硫酸,样品中的MnCO3和硫酸反应生成可溶性的MnSO4,滤液中含MnSO4,第②步发生5MnSO4+2NaClO3+4H2O=5MnO2↓+Cl2↑+Na2SO4+4H2SO4,第③步中发生氯气与热的NaOH发生氧化还原反应生成NaCl、NaClO3、水,溶液蒸发可得到固体,结合选项分析解答。
解析:由制备流程可知,MnO2不溶于硫酸,样品中的MnCO3和硫酸反应生成可溶性的MnSO4,滤液中含MnSO4,第②步发生5MnSO4+2NaClO3+4H2O=5MnO2↓+Cl2↑+Na2SO4+4H2SO4,第③步中发生氯气与热的NaOH发生氧化还原反应生成NaCl、NaClO3、水,溶液蒸发可得到固体,则
(1)只有MnO2不与硫酸反应,则MnO和MnCO3转化为可溶性物质;
(2)MnSO4要转化为MnO2,需失去电子,故需要加入NaClO3做氧化剂,依据得失电子守恒可以配平,所以反应的化学方程式是:5MnSO4+2NaClO3+4H2O=5MnO2↓+Cl2↑+Na2SO4+4H2SO4,因此反应的离子方程式是:2ClO3-+4H2O+5Mn2+=5MnO2↓+Cl2↑+8H+;
(3)流程中得到MnO2固体操作是过滤,必需的玻璃仪器有玻璃棒、烧杯、漏斗;
(4)Cl2通入热的NaOH溶液中一定发生氧化还原反应,且氯气既做氧化剂又做还原剂,NaClO3属于氧化产物,因此一定有还原产物NaCl;实验室制备氯气的离子方程式为4H++ MnO2+2Cl-![]() Cl2↑+Mn2++2H2O ;
Cl2↑+Mn2++2H2O ;
(5)由题意知样品中的MnO和MnCO3质量为50.76g-34.8 g=15.96g。0.896LCO2(标准状况下)是0.04mol,由方程式H2SO4+MnCO3=MnSO4+H2O+CO2↑可知MnCO3的物质的量为0.04mol,质量为115g/mol×0.04mol=4.6g,所以MnO的质量为15.96g-4.6g=11.36g,其物质的量为11.36g÷71g/mol=0.16mol,因此与稀硫酸反应时共生成MnSO4的物质的量为0.20mol,根据方程式5MnSO4+2NaClO3+4H2O=5MnO2↓+Cl2↑+Na2SO4+4H2SO4,可计算出需要NaClO3的物质的量为0.08mol,质量是0.08mol×106.5g/mol=8.52g;
(6)己知:①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-159.5kJ·mol-1
②NH2CO2NH4(s)=CONH2)2(s)+H2O(g) ΔH=+116.5kJ·mol-1
③H2O(l)=H2O(g) ΔH=+44.0kJ·mol-1
则根据盖斯定律可知①-②-③即得到CO2与NH3合成尿素和液态水的热化学反应方程式为2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l) ΔH=–87.0kJ·mol-1。

【题目】亚硝酸钠是一种工业盐,外观与食盐非常相似,毒性较强。
Ⅰ.经查:①Ksp(AgNO2)=2×10-8,Ksp(AgCl)=1.8×10-10;②Ka(HNO2)=5.1×10-4。请设计最简单的方法鉴别NaNO2和NaCl两种固体______________________
Ⅱ. 某小组同学用如下装置(略去夹持仪器)制备亚硝酸钠
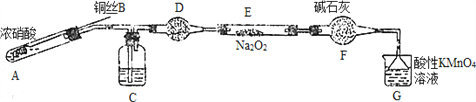
已知:①2NO+Na2O2=2NaNO2; ②酸性条件下,NO和NO2都能与MnO4-反应生成NO3-和Mn2+。
(1)使用铜丝的优点是________________________。
(2)装置A中发生反应的化学方程式为_____________________________。
装置C中盛放的药品是_________;(填字母代号)
A.浓硫酸 B.NaOH溶液 C.水 D.四氯化碳
(3)该小组称取5.000g制取的样品溶于水配成250ml溶液,取25.00ml溶液于锥形瓶中,
用0.1000mol·L-1酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
滴定次数 | 1 | 2 | 3 | 4 |
消耗KMnO4溶液体积/mL | 20.90 | 20.12 | 20.00 | 19.88 |
①第一次实验数据出现异常,造成这种异常的原因可能是_________(填字母代号)。
a.锥形瓶洗净后未干燥
b.酸式滴定管用蒸馏水洗净后未用标准液润洗
c.滴定终点时仰视读数
②酸性KMnO4溶液滴定亚硝酸钠溶液的离子方程式为___________________。
③该样品中亚硝酸钠的质量分数为______________。