题目内容
下列判断正确的是
A.酸酐一定是氧化物 | B.晶体中一定存在化学键 |
| C.碱性氧化物一定是金属氧化物 | D.正四面体分子中键角一定是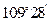 |
C
略

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
题目内容
A.酸酐一定是氧化物 | B.晶体中一定存在化学键 |
| C.碱性氧化物一定是金属氧化物 | D.正四面体分子中键角一定是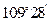 |

 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案