��Ŀ����
4��Cu��NO3��2����Ҫ�Ļ���ԭ�ϣ��ش����й�ҵ�����ͻ�ѧʵ���еļ������⣮��1��ʵ�������Ʊ�0.3mol Cu ��NO3��2���壬�ס�����ͬѧ�ֱ����ʵ�鷽�����£�
�ף�Cu $\stackrel{ϡHNO_{3}}{��}$ Cu��NO3��2�ң�Cu$\stackrel{O_{2}}{��}$CuO$\stackrel{ϡHNO_{3}}{��}$ Cu��NO3��2
����ɫ��ѧ�ĽǶȷ�������ͬѧ�ķ�������������ͬѧ�ɽ�Լ2mol/L��ϡ����100mL��
�ڼ��������ӷ���ʽΪ3Cu+8H++2NO3-=3Cu2++2NO��+4H2O
����ͬѧʵ��ʱͨ��O2�����ʲ��˹���Ϊ���ڹ۲�Ϳ��Ʋ���O2�����ʣ���ѡ��B������ĸ��ţ���

��Bװ����μ��������

��2��ijУ��ѧ��ȤС���ͬѧ������ͭ�����ȷֽ����̽���������������ͼ2װ�ü���Cu��NO3��2���壨���ȼ��г�װ��δ�����������ȹ��̷��֣�װ�â��еĹ�����Ϊ��ɫ��װ�â��������ݲ��������������Ĺ�������ʧ��ʯ����Һ��Ϊ��ɫ��Һ�弸������ѹ��װ�â��У���д��Cu��NO3��2���ȷֽ�Ļ�ѧ����ʽ��2Cu��NO3��2$\frac{\underline{\;����\;}}{\;}$CuO+4NO2��+O2����
��3��NO2��O2������NaNO3������ȼ�ϵ�أ���ԭ����ͼ3���õ����ʹ�ù�����ʯīI�缫������������Y����缫��ӦʽΪNO2+NO3--e-=N2O5��
���� ��1��������ʵ�鷽��Ҫ�ӷ�Ӧ�Ŀɲ����ԣ�����������ʣ��������ܵȷ����������ͬѧ��Cu $\stackrel{ϡHNO_{3}}{��}$ Cu��NO3���ķ������Ʊ�0.3mol Cu ��NO3��2���壬��������0.8mol����ͬѧ��Cu$\stackrel{O_{2}}{��}$CuO$\stackrel{ϡHNO_{3}}{��}$ Cu��NO3��2
�ķ������Ʊ�0.3mol Cu ��NO3��2���壬��������0.3mol���ݴ˼��㣻
��ͭ�ܽ���ϡ������������ͭ��NO��ˮ����ϵ����غ㡢����غ㼰ԭ���غ�д���˷�Ӧ�Ļ�ѧ����ʽ��
��ʵ��ʱͨ��O2�����ʲ��˹���Ϊ���ڹ۲�Ϳ��Ʋ���O2�����ʣ�����װ�ÿ�֪�����÷�Һ©�����Ƽ��������������ܴﵽҪ��
�ܼ��װ��B������ʱ���ɽ���������ѹǿ�γɵ�ˮ���ı仯���жϣ���������ƿ���������е��ɼл����K1��
��2��װ�â���Ҳ�����ݲ��������������Ĺ�������ʧ��˵���������ж���������������װ�â��еĹ�����Ϊ��ɫ��˵��������������ͭ����Ȼ����������غ���ƽ��
��3����ԭ�����ͨ����������ĵ缫�Ǹ�����ͨ�������ĵ缫������������I�Ǹ�����II�����������������������Ӧ���Ƕ�������ʧ���Ӻ���������ӷ�Ӧ����������������
��� �⣺��1��������ʵ�鷽��Ҫ�ӷ�Ӧ�Ŀɲ����ԣ�����������ʣ��������ܵȷ����������ͬѧ��Cu $\stackrel{ϡHNO_{3}}{��}$ Cu��NO3���ķ������Ʊ�0.3mol Cu ��NO3��2���壬��������0.8mol����ͬѧ��Cu$\stackrel{O_{2}}{��}$CuO$\stackrel{ϡHNO_{3}}{��}$ Cu��NO3��2
�ķ������Ʊ�0.3mol Cu ��NO3��2���壬��������0.6mol��������ͬѧ��Լ2mol/L��ϡ��������Ϊ$\frac{0.8-0.6}{2}$L=100mL��
�ʴ�Ϊ���ң�100��
��Cu�ܽ���ϡ���ᷢ����Ӧ�����ӷ���ʽΪ3Cu+8H++2NO3-=3Cu2++2NO��+4H2O���ʴ�Ϊ��3Cu+8H++2NO3-=3Cu2++2NO��+4H2O��
��ʵ��ʱͨ��O2�����ʲ��˹���Ϊ���ڹ۲�Ϳ��Ʋ���O2�����ʣ�����װ�ÿ�֪�����÷�Һ©�����Ƽ��������������ܴﵽҪ��װ��B�����ɵ�����ͨ��Ũ������Ը���������ͬʱ�۲���������ð�������ʿ����������������ʣ�����ѡ��Bװ�ã�
�ʴ�Ϊ��B��
�ܿ�ͨ���ر�K1����Һ©���Ļ�����ע��ˮ���۲�©����ˮ���½�����һ���߶ȱ��ֲ��䣬˵��Bװ�����������ã��ʴ�Ϊ���ر�K1����Һ©���Ļ�����ע��ˮ���۲�©����ˮ���½�����һ���߶ȱ��ֲ��䣬˵�����������ã�
��2�����ȵ���Cu��NO3��2�����ȹ��̷��֣�װ�â���Ҳ�����ݲ��������������Ĺ�������ʧ��ʯ����Һ��Ϊ��ɫ��Һ�弸������ѹ��װ�â��У�˵����������������ǡ����ˮ��Ӧ�������ᣬװ�â��еĹ�����Ϊ��ɫ��˵����������ͭ����ʽΪ��2Cu��NO3��2$\frac{\underline{\;����\;}}{\;}$CuO+4NO2��+O2����
�ʴ�Ϊ��2Cu��NO3��2$\frac{\underline{\;����\;}}{\;}$CuO+4NO2��+O2����
��3����ԭ�����ͨ����������ĵ缫�Ǹ�����ͨ�������ĵ缫������������I�Ǹ�����II�����������������������Ӧ���Ƕ�������ʧ���Ӻ���������ӷ�Ӧ�����������������缫��ӦʽΪNO2+NO3--e-=N2O5��
�ʴ�Ϊ��NO2+NO3--e-=N2O5��
���� ���⿼�������ʳɷ�̽��ʵ��͵绯ѧ�����֪ʶ����Ŀ�漰��֪ʶ��Ƚ϶࣬����һ����Ӧ�Ŀ�����Ҫ�Ӷ���������ӷ�Ӧ�Ŀ����ԣ�������ȫ��������㣬���ý��ܷ��濼�ǣ������ѶȽϴ�

 �ǻۿ����ܾ�100�ֵ�Ԫ���ؼ��ϵ�д�
�ǻۿ����ܾ�100�ֵ�Ԫ���ؼ��ϵ�д�| A�� | �Ʊ�����װ���еķ�Һ©�� | B�� | �Ʊ�Fe��OH��2�����еĽ�ͷ�ι� | ||
| C�� | ����ʯ��ʱ���¶ȼ� | D�� | ���Ȼ�����������ˮʱ�ĵ��� |
| A�� | ���ʯ��ʯī�ȶ� | B�� | ʯī�ͽ��ʯ��̼Ԫ�ص�ͬλ�� | ||
| C�� | 1molʯī��1mol���ʯ���������� | D�� | ���ʯת��Ϊʯī���ڻ�ѧ�仯 |
 ���Ⱦ۱�ϩ�����Ͽ��Եõ�̿�����������顢��ϩ����ϩ�����ͼױ�������ͼ��ʾװ��̽���Ͼ����ϵ������ã�������������ȷ���ǣ�������
���Ⱦ۱�ϩ�����Ͽ��Եõ�̿�����������顢��ϩ����ϩ�����ͼױ�������ͼ��ʾװ��̽���Ͼ����ϵ������ã�������������ȷ���ǣ�������| A�� | ��ϩ�����й��õ��Ӷ���Ϊ5 | B�� | װ��B���Թ��п��ռ����� | ||
| C�� | װ��C�е��Լ�������ϩ�� | D�� | ����ռ����������ȼ�� |
| A�� | ������C4H8�ĺ˴Ź����������Ϊ4 | |
| B�� | ��ѧʽΪC8H8���л��һ����ʹ���Ը��������Һ��ɫ | |
| C�� |  ��ͬ���칹���У������д��ࡢ��û�з������� ��ͬ���칹���У������д��ࡢ��û�з������� | |
| D�� | 1 mol 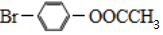 �������2 mol NaOH��Ӧ �������2 mol NaOH��Ӧ |
| A�� | 1��7 | B�� | 6��8 | C�� | 11��16 | D�� | 12��17 |

 ��
�� ���ܷ�Ӧ����b��������ĸ��
���ܷ�Ӧ����b��������ĸ��