题目内容
20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成,而是在反应物到生成物的过程中经过一个高能量的过渡态.

(1)图I是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是
(2)图Ⅱ是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:
(3)下表是部分化学键的键能数据:
已知白磷的燃烧热为2982kJ/mol,白磷(P4)、P4O6、P4O10结构如下图所示,则上表中X=
(4)0.5mol白磷(P4)与O2完全反应生成固态P4O6放出的热量为

(1)图I是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是
C
C
(选填“A”、“B”或“C”);(2)图Ⅱ是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:
NO2(g)+CO(g)=CO2(g)+NO(g);△H=-234kJ/mol
NO2(g)+CO(g)=CO2(g)+NO(g);△H=-234kJ/mol
;(3)下表是部分化学键的键能数据:
| 化学键 | P-P | P-O | O=O | P=O |
| 键能/kJ?mol-1 | 198 | 360 | 498 | X |
585
585
.(4)0.5mol白磷(P4)与O2完全反应生成固态P4O6放出的热量为
819
819
kJ.分析:(1)发生化学反应的碰撞才是有效碰撞;
(2)反应物总能量大于生成物总能量,反应放热,根据活化能之差计算反应热;
(3)根据反应热等于反应物的总键能与生成物的总键能之差,结合反应热计算键能;
(4)根据反应热等于反应物的总键能与生成物的总键能之差计算.
(2)反应物总能量大于生成物总能量,反应放热,根据活化能之差计算反应热;
(3)根据反应热等于反应物的总键能与生成物的总键能之差,结合反应热计算键能;
(4)根据反应热等于反应物的总键能与生成物的总键能之差计算.
解答:解:(1)发生化学反应的碰撞才是有效碰撞,根据图可知只有C发生化学变化,则C发生有效碰撞,故答案为:C;
(2)反应物总能量大于生成物总能量,反应放热,反应热等于134kJ/mol-368kJ/mol=-234kJ/mol,
则热化学方程式为NO2(g)+CO(g)=CO2(g)+NO(g);△H=-234 kJ/mol,
故答案为:NO2(g)+CO(g)=CO2(g)+NO(g);△H=-234 kJ/mol;
(3)白磷燃烧的热化学方程式为P4(s)+5O2(g)=P4O10(s)△H=-2982kJ/mol,
则6×198kkJ/mol+5×498kJ/mol-12×360kJ/mol-4X=-2982kJ/mol,
X=585kJ/mol,
故答案为:585;
(4)白磷燃烧生成P4O6的热化学方程式为P4(s)+3O2(g)=P4O6(s);
△H=6×198kkJ/mol+3×498kJ/mol-12×360kJ/mol=-1638kJ/mol,
则0.5mol白磷(P4)与O2完全反应生成固态P4O6放出的热量为0.5mol×1638kJ/mol=819kJ,
故答案为:819.
(2)反应物总能量大于生成物总能量,反应放热,反应热等于134kJ/mol-368kJ/mol=-234kJ/mol,
则热化学方程式为NO2(g)+CO(g)=CO2(g)+NO(g);△H=-234 kJ/mol,
故答案为:NO2(g)+CO(g)=CO2(g)+NO(g);△H=-234 kJ/mol;
(3)白磷燃烧的热化学方程式为P4(s)+5O2(g)=P4O10(s)△H=-2982kJ/mol,
则6×198kkJ/mol+5×498kJ/mol-12×360kJ/mol-4X=-2982kJ/mol,
X=585kJ/mol,
故答案为:585;
(4)白磷燃烧生成P4O6的热化学方程式为P4(s)+3O2(g)=P4O6(s);
△H=6×198kkJ/mol+3×498kJ/mol-12×360kJ/mol=-1638kJ/mol,
则0.5mol白磷(P4)与O2完全反应生成固态P4O6放出的热量为0.5mol×1638kJ/mol=819kJ,
故答案为:819.
点评:本题主要考查反应热的计算,题目难度中等看,解答本题的关键是把握如何利用键能计算反应热,注意相关计算方法的运用.学习中注意体会.

练习册系列答案
相关题目
(8分)(1)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。如图是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是 (填“吸热”或“放热”)反应,NO2和CO的总能量 (填“>”、“<”或“=”)CO2和NO的总能量。
(2)在某体积为2L的密闭容器中充入0.5mol NO2和1mol CO,在一定条件下发生反应:NO2+CO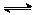 CO2+NO,2 min时,测得容器中NO的物质的量为0.2 mol ,则:
CO2+NO,2 min时,测得容器中NO的物质的量为0.2 mol ,则:
①该段时间内,用CO2表示的平均反应速率为 。
②假设此反应在5 min时达到平衡,则此时容器内气体的总物质的量为 。
③下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是
| A.容器内气体的质量保持变 | B.NO2的物质的量浓度不再改变 |
| C.容器内气体的平均相对分子质量不变 | D.NO2的消耗速率与CO2的消耗速率相等 |
 (1)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态.如图是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是
(1)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态.如图是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是 CO2+NO,2min时,测得容器中NO的物质的量为0.2mol,则:
CO2+NO,2min时,测得容器中NO的物质的量为0.2mol,则:
 CO2+NO,2 min时,测得容器中NO的物质的量为0.2 mol ,则:
CO2+NO,2 min时,测得容器中NO的物质的量为0.2 mol ,则:
 CO2+NO,2 min时,测得容器中NO的物质的量为0.2 mol ,则:
CO2+NO,2 min时,测得容器中NO的物质的量为0.2 mol ,则: