题目内容
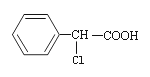
【题目】常温下,Ksp(CaSO4)=9×10﹣6 , CaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( ) 
A.CaSO4在稀硫酸中的溶解性比在纯水中的溶解性强
B.a点对应的Ksp等于c点对应的Ksp
C.d点溶液通过蒸发可以变到c点
D.b点将有沉淀生成,平衡后溶液中c(SO42﹣)一定等于3×10﹣3mol/L
【答案】B
【解析】解:A.稀硫酸使溶解平衡逆向移动,则CaSO4在稀硫酸中的溶解性比在纯水中的溶解性弱,故A错误;
B.曲线上的点为平衡点,且温度不变,则a点对应的Ksp等于c点对应的Ksp,故B正确;
C.蒸发时离子浓度增大,则d点溶液不能通过蒸发可以变到c点,因d、c点硫酸根离子浓度相同,故C错误;
D.b转化为a或转化为c,均有沉淀生成,则平衡后溶液中c(SO42﹣)可能等于3×10﹣3mol/L、5×10﹣3mol/L、4×10﹣3mol/L,故D错误;
故选B.

 阅读快车系列答案
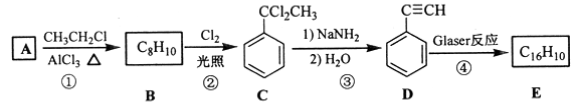
阅读快车系列答案【题目】正丁醛是一种化工原料。某实验小组利用如图装置合成正丁醛.发生的反应如下:![]() 。
。
反应物和产物的相关数据列表如下:
沸点/℃ | 密度/(gcm-3) | 水中溶解性 | |
正丁醇 | 117.2 | 0.8109 | 微溶 |
正丁醛 | 75.7 | 0.8017 | 微溶 |
已知:醛基可被酸性Na2Cr2O7氧化。
实验步骤如下:
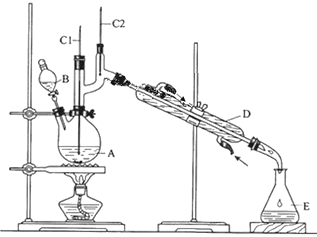
将6.0gNa2Cr2O7放入100mL烧杯中,加水30mL溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中。在A中加入4.0g正丁醇和几粒沸石,加热。当有蒸汽出现时,开始滴加B中溶液。滴加过程中保持反应温度为90~95℃,在E中收集90℃以上的馏分。将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77℃馏分,产量2.0g。回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,说明理由__________________。
(2)加入沸石的作用是______________,若加热后发现未加入沸石,应采取的正确措施是______________________________。
(3)上述装置图中,B仪器的名称是_____________,D仪器的名称是_______________。
(4)反应温度应保持在90~95℃,其原因是___________________________。
(5)温度计C1的作用_________________,C2的作用_______________。
(6)本实验中,正丁醛的产率为_________%。
【题目】某学生用0.2000molL﹣1的标准NaOH溶液滴定未知浓度的盐酸,其操作如下: ①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“0”或“0”刻度线稍下,并记下读数;
④移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数.
请回答:
(1)以上步骤有错误的是(填编号) , 该错误操作会导致测定结果(填“偏大”、“偏小”或“无影响”) .
(2)判断滴定终点的现象是: .
(3)如图是某次滴定时的滴定管中的液面,其读数为mL. ![]()
(4)根据下列数据:请计算待测盐酸溶液的浓度:mol/L.
滴定次数 | 待测体积(mL) | 标准烧碱体积(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 20.00 | 0.40 | 20.40 |
第二次 | 20.00 | 2.00 | 24.10 |
第三次 | 20.00 | 4.00 | 24.00 |
【题目】太阳能、风能发电逐渐得到广泛应用,在发电系统中安装储能装置有助于持续稳定供电,其构造的简化图如下:

(1)下列说法中,正确的是______( 填字母序号)。
a.太阳能、风能都是清洁能源
b.太阳能电池组实现了太阳能到电能的转化
c.控制系统能够控制储能系统是充电还是放电
d.阳光或风力充足时,储能系统实现由化学能到电能的转化
(2)全钒液流电池是具有发展前景的、用作储能系统的蓄电池。已知放电时V2+发生氧化反应,则放电时电极A 的电极反应式为___________;充电时电极B 做______极。
(3)含钒废水会造成水体污染,对含钒废水(除VO2+外,还含有Al3+,Fe3+等)进行综合处理可实现钒资源的回收利用,流程如下:
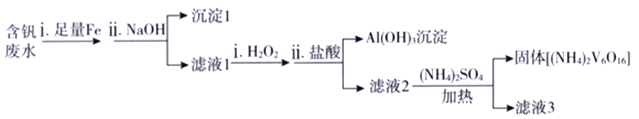
已知溶液pH 范围不同时,钒的存在形式如下表所示:
钒的化合价 | pH<2 | pH>11 |
+4价 | VO2+,VO(OH)+ | VO(OH)3- |
+5价 | VO2+ | VO43- |
①加入NaOH 调节溶液pH至13时,沉淀1达最大量,并由灰白色转变为红褐色,用化学用语表示加入NaOH 后生成沉淀1的反应过程为_______、_______;所得滤液1中,铝元素的存在形式为__________。
②向碱性的滤液1( V的化合价为+4 )中加入H2O2的作用是________(用离子方程式表示)。