题目内容
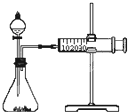 影响化学反应速率的因素很多,某同学设计了以下实验研究不同浓度的硫酸对反应速率的影响.药品:Cu、Fe、Na和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L);装置如图.
影响化学反应速率的因素很多,某同学设计了以下实验研究不同浓度的硫酸对反应速率的影响.药品:Cu、Fe、Na和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L);装置如图.(1)用此装置进行定量实验,应选用上述的实验药品是:
Fe、0.5mol/L硫酸、2mol/L硫酸
Fe、0.5mol/L硫酸、2mol/L硫酸
;(2)应该测定的实验数据是
测定一定时间产生的体积(或者测定一定体积的气体所需的时间)
测定一定时间产生的体积(或者测定一定体积的气体所需的时间)
;(3)此实验忽视了影响反应速率的其他因素是(假设金属颗粒是均匀的):
温度对反应速率的影响
温度对反应速率的影响
.分析:(1)该装置为固体和液体反应,且不需要加热,据此即可解答;
(2)根据实验的目的研究不同浓度的硫酸对反应速率的影响出发进行解答;
(3)金属和酸反应是放热反应,温度越高,反应的速率越大;
(2)根据实验的目的研究不同浓度的硫酸对反应速率的影响出发进行解答;
(3)金属和酸反应是放热反应,温度越高,反应的速率越大;
解答:解:(1)该装置左边为分夜漏斗,锥形瓶,分液漏斗为加液体,锥形瓶为反应容器,右边为量气装置,且该装置不需加热,该实验的目的为探究不同浓度的硫酸对反应速率的影响,进行的是定量实验,所以需选用的实验药品为统一溶质硫酸不同浓度与较活泼的金属固体反应,故答案为:Fe、0.5mol/L硫酸、2mol/L硫酸;
(2)反应速率的表示方法为单位时间内反应物浓度的减少,或生成物浓度的增加.探究不同浓度的硫酸对反应速率的影响,所以可以测生成物气体的体积或生成气体所需的时间,故答案为:测定一定时间产生的体积(或者测定一定体积的气体所需的时间);
(3)影响反应速率的因素有:浓度、温度、气体的压强、固体的表面积大小、催化剂等.该实验假设金属颗粒是均匀的已考虑表面积,该实验未用催化剂,所以应考虑热效应,金属与酸反应为典型的放热反应,所以硫酸浓度大的,反应放出的热量大,温度相对高一点,温度高反应速率快,所以该实验为考虑温度对反应速率的影响,故答案为:温度对反应速率的影响;
(2)反应速率的表示方法为单位时间内反应物浓度的减少,或生成物浓度的增加.探究不同浓度的硫酸对反应速率的影响,所以可以测生成物气体的体积或生成气体所需的时间,故答案为:测定一定时间产生的体积(或者测定一定体积的气体所需的时间);
(3)影响反应速率的因素有:浓度、温度、气体的压强、固体的表面积大小、催化剂等.该实验假设金属颗粒是均匀的已考虑表面积,该实验未用催化剂,所以应考虑热效应,金属与酸反应为典型的放热反应,所以硫酸浓度大的,反应放出的热量大,温度相对高一点,温度高反应速率快,所以该实验为考虑温度对反应速率的影响,故答案为:温度对反应速率的影响;
点评:本题主要考查学生的实验探究能力,解答时须注意实验的原理,难度中等.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
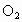 中比在空气中燃烧剧烈._______
中比在空气中燃烧剧烈._______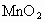 加入双氧水中反应更剧烈________
加入双氧水中反应更剧烈________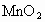 加入
加入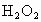 中反应更加剧烈__________.
中反应更加剧烈__________.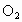 中比在空气中燃烧剧烈._______
中比在空气中燃烧剧烈._______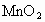 加入双氧水中反应更剧烈________
加入双氧水中反应更剧烈________