题目内容
(9分)(1)1 mol气态钠离子和1 mol气态氯离子结合生成1 mol氯化钠晶体释放出的热能为氯化钠晶体的晶格能。
①下列热化学方程式中,能直接表示出氯化钠晶体晶格能的是____________。
A.Na+(g)+Cl-(g)―→NaCl(s);△Q
B.Na(s)+Cl2(g)―→NaCl(s);△Q1
C.Na(s)―→Na(g);△Q2
D.Na(g)-e-―→Na+(g);△Q3
E.Cl2(g)―→Cl(g);△Q4
F.Cl(g)+e-―→Cl-(g);△Q5
②写出△Q1与△Q、△Q2、△Q3、△Q4、△Q5之间的关系式________________________________________________________________________
(2)可逆反应:aA(g)+bB(g)  ??cC(g)+dD(g),取a mol A和b mol B置于V L密闭容器中,2
min后,测得容器中A的浓度为x mol·L-1,以物质C的浓度变化来表示这段时间内反应的平均速率应为__________ __。
??cC(g)+dD(g),取a mol A和b mol B置于V L密闭容器中,2
min后,测得容器中A的浓度为x mol·L-1,以物质C的浓度变化来表示这段时间内反应的平均速率应为__________ __。
【答案】
(1) ①A ②△Q1=△Q+△Q2+△Q3+△Q4+△Q5
(2) mol/(L·min)
【解析】略

练习册系列答案
相关题目
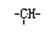 和a 个—CH3,其余为—OH,则—OH 的个数为
和a 个—CH3,其余为—OH,则—OH 的个数为