题目内容
11.设NA为阿伏伽德罗常数的值.下列叙述正确的是( )| A. | 标准状况下,0.56 L丙烷中含有共价键的数目为0.2NA | |
| B. | 0.1 mol SO2与0.2 mol O2充分反应后可得到0.1NA个SO3分子 | |
| C. | 2.24 L 氯气与足量钠反应时转移电子数目为0.2NA | |
| D. | 0.1 mol乙烯和乙醇(蒸气)混合物完全燃烧所消耗的氧原子数一定为0.6NA |
分析 A、标况下,0.56L丙烷的物质的量为0.025mol,而1mol丙烷中含10mol共价键;
B、SO2与 O2的反应为可逆反应;
C、氯气所处的状态不明确;
D、1mol乙烯和1mol乙醇的耗氧量均为3mol.
解答 解:A、标况下,0.56L丙烷的物质的量为0.025mol,而1mol丙烷中含10mol共价键,故0.025mol丙烷中含0.25mol共价键,即0.25NA个,故A错误;
B、SO2与 O2的反应为可逆反应,不能进行彻底,故生成的三氧化硫分子个数小于0.1NA个,故B错误;
C、氯气所处的状态不明确,故氯气的物质的量不能计算,故C错误;
D、1mol乙烯和1mol乙醇的耗氧量均为3mol,故0.1mol乙烯和乙醇的混合蒸汽一定消耗0.3mol氧气即0.6mol氧原子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
1.某烃的结构简式为: 它可能具有的性质是( )
它可能具有的性质是( )
 它可能具有的性质是( )
它可能具有的性质是( )| A. | 易溶于水,也易溶于有机溶剂 | |
| B. | 能发生聚合反应,其产物可表示为: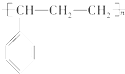 | |
| C. | 能使溴水褪色,但不能使酸性KMnO4溶液褪色 | |
| D. | 既能使溴水褪色,又能使酸性KMnO4溶液褪色 |
2.设 NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
| A. | 7.8 gNa2O2含有的阴离子数目为 0.2NA | |
| B. | 56gFe 与稀 H N03 完全反应时一定转移3NA个电子 | |
| C. | 1 molC10H22分子中共价键总数为 3lNA | |
| D. | 已知热化学方程式2SO2(g)+O2?(g)2SO(g) 3△=-QkJ/mol(Q>0),则将 2NA 个SO2分子和 NA 个O2分子置于一密闭容器中充分反应后放出QkJ的热量 |
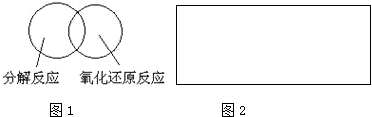
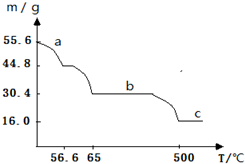 FeSO4是一种精细化工产品,可用于治疗缺铁性贫血、制革、木材防腐等.制备步骤:①将3mol•L-1硫酸加入铁粉里,微热,搅拌使其充分反应;②趁热过滤;③在50℃左右蒸发、结晶,得到晶体--绿矾(FeSO4•7H2O).回答下列问题:
FeSO4是一种精细化工产品,可用于治疗缺铁性贫血、制革、木材防腐等.制备步骤:①将3mol•L-1硫酸加入铁粉里,微热,搅拌使其充分反应;②趁热过滤;③在50℃左右蒸发、结晶,得到晶体--绿矾(FeSO4•7H2O).回答下列问题: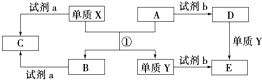
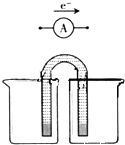 Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液.
Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液.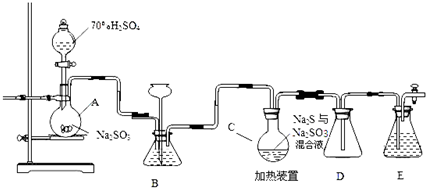
 .
.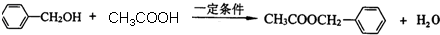 .
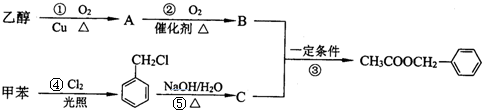
.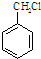 为原料经过三步反应合成
为原料经过三步反应合成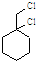 ,无机原料任选,写出反应的化学方程式:
,无机原料任选,写出反应的化学方程式: +H2$→_{△}^{催化剂}$
+H2$→_{△}^{催化剂}$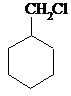
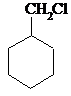 +NaOH$→_{△}^{乙醇}$
+NaOH$→_{△}^{乙醇}$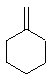 +NaCl+H2O
+NaCl+H2O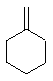 +Cl2→
+Cl2→ .
.