题目内容
|
下列叙述中正确的是 | |
A. |
22.4 L任何气体的物质的量均为1 mol |
B. |
非标准状况下1 mol任何气体不可能占有22.4 L体积 |
C. |
1 mol气体在25℃、101 kPa下的体积肯定大于22.4 L |
D. |
在同温同压下,相同质量的CO和N2具有相同的体积 |
答案:CD
解析:
解析:
|
A项22.4 L气体在标准状况下物质的量为1 mol. B项非标准状况下,通过调节温度和压强,可以使1 mol气体的体积为22.4 L. C项1 mol气体在101 kPa、25℃时体积大于22.4 L,因为温度升高(0℃→25℃),气体体积变大. D项相同条件下,m(CO)=m(N2),且M(CO)=M(N2)=28 g·mol-1. 所以n(CO)=n(N2),故V(CO)=V(N2). |

练习册系列答案
相关题目
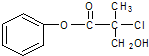 有机物A是农药生产中的一种中间体,结构简式如图所示.下列叙述中正确的是( )
有机物A是农药生产中的一种中间体,结构简式如图所示.下列叙述中正确的是( )| A、有机物A可以在一定条件下与HBr发生反应 | B、1mol A最多能与4mol H2发生加成反应 | C、有机物A与浓硫酸混合加热,可以发生消去反应 | D、1mol A与足量的NaOH溶液反应,最多可以消耗3mol NaOH |


