题目内容
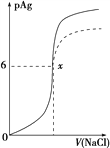
【题目】已知:pAg=-lg c(Ag+),Ksp(AgCl)=1×10-12。如图是向10 mL AgNO3溶液中逐渐加入0.1 mol/L的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位:mL)变化的图像(实线)。根据图像所得下列结论正确的是
A. 原AgNO3溶液的物质的量浓度为也为0.1 mol·L-1
B. 图中x点的坐标为(10,6)
C. 图中x点可认为溶液中Ag+被沉淀完全
D. 把0.1 mol·L-1的NaCl换成0.1 mol·L-1NaI,则图像在终点后变为虚线部分
【答案】C
【解析】A、图中原点pAg=0,Ag+的浓度为:c(Ag+)=100 molL-1,原AgNO3溶液的物质的量浓度为1 molL-1,故A错误;B、一般认为溶液中离子浓度小于10-5 molL-1,即沉淀完全。x点c(Ag+)=10-6 molL-1,则AgNO3与NaCl恰好反应,n(NaCl)=n(AgNO3)=0.01L×1molL-1=0.01mol,所以V(NaCl)=100mL,即x点的坐标为(100,6),故B错误;C、x点c(Ag+)=10-6 molL-1,一般认为溶液中离子浓度小于10-5 molL-1完全沉淀,实际上Ag+没有完全沉淀,是处于沉淀与溶解的平衡状态,故C正确;D、与AgCl相比,碘化银的Ksp(AgI)更小,所以把0.1 molL-1的NaCl换成0.1molL-1NaI,则溶液中c(Ag+)更小,则pAg更大,图象不符,故D错误;故选C。

练习册系列答案
相关题目