题目内容
已知298K时下述反应:
①C(s)+1/2O2(g)=CO(g)△H1=-110.5kJ?mol-1
②CO(g)+1/2O2(g)=CO2(g)△H2=-283.0kJ?mol-1
③C(s)+CO2(g)=2CO(g)△H3,
则△H3等于( )
①C(s)+1/2O2(g)=CO(g)△H1=-110.5kJ?mol-1
②CO(g)+1/2O2(g)=CO2(g)△H2=-283.0kJ?mol-1
③C(s)+CO2(g)=2CO(g)△H3,
则△H3等于( )
分析:依据热化学方程式和盖斯定律计算分析,反应焓变与反应过程无关,与起始和终了状态有关.
解答:解:①C(s)+1/2O2(g)=CO(g)△H1=-110.5kJ?mol-1
②CO(g)+1/2O2(g)=CO2(g)△H2=-283.0kJ?mol-1
依据盖斯定律①-②得到:C(s)+CO2(g)=2CO(g)△H3=172.5 kJ?mol-1
故选A.
②CO(g)+1/2O2(g)=CO2(g)△H2=-283.0kJ?mol-1
依据盖斯定律①-②得到:C(s)+CO2(g)=2CO(g)△H3=172.5 kJ?mol-1
故选A.
点评:本题考查了热化学方程式和盖斯定律的计算应用明天买较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 已知298K时:
已知298K时: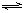 2NH3(g)ΔH=-92.2kJ?mol-1 ΔS=-198.2J?mol-1?K-1。
2NH3(g)ΔH=-92.2kJ?mol-1 ΔS=-198.2J?mol-1?K-1。