题目内容
18.下列说法错误的是(NA为阿伏加德罗常数的数值)( )| A. | 常温常压下,1molN2含有NA个分子 | |
| B. | 标准状况下,22.4LCH4含有约4NA个氢原子 | |
| C. | 1molK2SO4溶于足量的水中后,溶液中含有2NA个K+ | |
| D. | 1molCH4比1molH2O的分子数多 |
分析 A、分子个数N=nNA来计算;
B、标况下,22.4L甲烷为1mol;
C、1mol硫酸钾含2mol钾离子;
D、分子个数和物质的量成正比.
解答 解:A、分子个数N=nNA=1mol×NA/mol=NA,故A正确;
B、标况下,22.4L甲烷为1mol,而1mol甲烷中含4mol氢原子即4NA个,故B正确;
C、1mol硫酸钾含2mol钾离子,故1molK2SO4溶于足量的水中后,溶液中含有2NA个K+,故C正确;
D、分子个数和物质的量成正比,故当甲烷和水的物质的量相等时,两者的分子个数相等,故D错误.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
8.食品香精“菠萝酯”的生产路线(反应条件略去)如下.下列叙述正确的是( )


| A. | 苯氧乙酸与菠萝酯互为同系物 | |
| B. | 苯酚、苯氧乙酸和菠萝酯均可与NaOH溶液发生反应 | |
| C. | 步骤(1)产物中残留的苯酚可用FeCl3溶液检验 | |
| D. | 步骤(2)产物中残留的烯丙醇可用溴水检验 |
9.下列各组物质,互为同系物的是( )
| A. | CH3-CH=CH2与 | B. |  与 与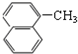 | ||
| C. |  与 与 | D. | CH3CH2Cl与CH3CHCl-CH2Cl |
6.下列物质中含氢原子个数最多的是( )
| A. | 3.01×1023个CH4分子 | B. | 4℃时23.4mL H2O | ||
| C. | 23g C2H5OH | D. | 常温常压下22.4LNH3 |
13.下列对物质的量及其单位的理解正确的是( )
| A. | 物质的量即物质的数量 | |
| B. | 物质的量是国际基本物理量之一 | |
| C. | 摩尔是一个物理量 | |
| D. | 1mol任何物质都含有6.02×1023个原子 |
3.甲、乙、丙、X是中学化学中常见的4种物质,其转化关系符合如图.其中甲和X可能是( )


| A. | 甲为Fe、X为Cl2 | B. | 甲为S、X为O2 | ||
| C. | 甲为SO2、X为NaOH溶液 | D. | 甲为AlCl3溶液、X为NH3•H2O |
10.在两个容积相同的容器中,一个盛有C2H4气体,另一个盛有N2和CO的混合气体.在同温同压下,两容器内的气体一定相同的物理量有几项( )
(1)分子数 (2)原子数 (3)质量 (4)电子数 (5)密度 (6)摩尔质量 (7)气体摩尔体积.
(1)分子数 (2)原子数 (3)质量 (4)电子数 (5)密度 (6)摩尔质量 (7)气体摩尔体积.
| A. | 4项 | B. | 5项 | C. | 6项 | D. | 7项 |
12.将等物质的量的A、B混合于1L的密闭容器中,发生反应:2A(g)+B(g)?2C(g)+D(?),5min时,测得密闭容器内气体压强减小,且c(A):c(B)=3:4,5min内,v(A)=0.2mol•L-1•minL-1,下列有关结论正确的是( )
| A. | D为气体 | B. | B的转化率为80% | ||
| C. | 5min时,c(A)=1.5mol•L-1 | D. | 反应开始前A的物质的量为2mol |