题目内容
【题目】下表是元素周期表中部分元素,请回答下列问题:
IA | IIA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 | |
1 | H | He | ||||||
2 | Li | C | N | O | F | |||
3 | Na | Al | Si | S | Cl |
(1)上表所列元素中,属于金属元素的有_____种,金属性最强的元素与氧反应生成的化合物有Na2O和________(填化学式)。
(2)上表所列元素中,化学性质最不活泼的是_____,非金属性最强的元素形成的单质的电子式为__________。
(3)N、C、Si三种元素的气态氢化物中,最稳定的是______(化学式)。
(4)上表所列的第三周期的元素中,原子半径最小的是_______。
【答案】(1)3;Na2O2;(2)He;![]() ;(3)NH3;(4)Cl。
;(3)NH3;(4)Cl。
【解析】试题分析:(1)上表所列元素中,属于金属元素的有Li、Na、Al三种元素;由于同一周期的元素,原子序数越大,元素的金属性越弱;同一主族的元素,原子序数越大,元素的金属性越强,所以上述三种金属元素中金属性最强的元素是Na,其形成的氧化物有Na2O和Na2O2;(2)上表所列元素中,化学性质最不活泼的是惰性气体元素He;非金属性最强的元素是F,该原子最外层有7个电子,两个F原子形成一对共用电子,从而使分子中每个原子都达到8个电子的稳定结构,形成的单质的电子式为![]() ;(3)N、C、Si三种元素的非金属性强弱顺序是N>C>Si,元素的非金属性越强,其相应的气态氢化物的稳定性就越强。所以三种元素的气态氢化物中,最稳定的是NH3;(4)由于同一周期的元素,原子序数越大,元素的原子半径越小,所以上表所列的第三周期的元素中,原子半径最小的是Cl元素。
;(3)N、C、Si三种元素的非金属性强弱顺序是N>C>Si,元素的非金属性越强,其相应的气态氢化物的稳定性就越强。所以三种元素的气态氢化物中,最稳定的是NH3;(4)由于同一周期的元素,原子序数越大,元素的原子半径越小,所以上表所列的第三周期的元素中,原子半径最小的是Cl元素。

【题目】(1)对于反应2S02(g)+O2(g)=2SO3(g),当其他条件不变时,只改变一个反应条件。将生成SO3的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”)。
编号 | 改变的条件 | 生成SO3的速率 |
① | 降低温度 | |
② | 压缩体积 | |
③ | 使用催化剂 |
(2)用铜片、锌片和稀硫酸及若干其他器材组合成一个原电池.如图所示。回答下列问题:
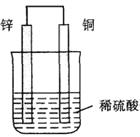
① 该原电池装置将_______(选填“化学能转化为电能”或“电能转化为化学能”);
② 此电池的负极是______,正极的电极反应方程式是________。
③ 该电池工作一段时间,将两个电极小心取出洗涤并晾干,经称量发现锌片比原来减少6.5g(锌的相对原子质量为:65)。请计算理论上导线中共通过了____mol电子。