题目内容
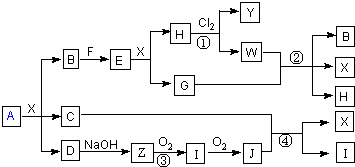
从由两种正盐组成的混合物A的水溶液出发,有如图所示的一系列变化.其中B、F为固态单质,其余为化合物.B呈黄色,C、G、Z、I、J常温下是气体,Y、W的阳离子相同.(参与反应或生成的水均没有标出).

回答下列问题:
(1)组成A的两种盐的化学式为
(2)写出①的离子方程式
(3)写出②的离子方程式
(4)写出③的化学反应方程式
(5)写出④的化学反应方程式
(6)写出实验室检验D中阳离子的操作和现象.
(7)将Y溶液滴入沸水可得到红褐色液体,反应的离子方程式是:
a.光束通过该液体时形成光亮的“通路”
b.插入电极通直流电后,有一极附近液体颜色加深
c.向该液体中加入稀硫酸溶液,先有沉淀产生,后沉淀溶解
d.将该液体加热、蒸干、灼烧后,有氢氧化物生成.

回答下列问题:
(1)组成A的两种盐的化学式为
(NH4)2S
(NH4)2S
和(NH4)2SO3
(NH4)2SO3
.(2)写出①的离子方程式
2Fe2++Cl2=2Fe3++2Cl-
2Fe2++Cl2=2Fe3++2Cl-
.(3)写出②的离子方程式
2Fe3++H2S=S↓+2Fe2++2H+
2Fe3++H2S=S↓+2Fe2++2H+
.(4)写出③的化学反应方程式
4NH3+5O2
4NO+6H2O
| ||
4NH3+5O2
4NO+6H2O
.
| ||
(5)写出④的化学反应方程式
NO2+SO2+H2O=H2SO4+NO
NO2+SO2+H2O=H2SO4+NO
.(6)写出实验室检验D中阳离子的操作和现象.
取样品D于试管中,加入NaOH溶液,加热.用湿润的红色石蕊试纸在试管口检验,若红色石蕊试纸变蓝,说明有NH4+
取样品D于试管中,加入NaOH溶液,加热.用湿润的红色石蕊试纸在试管口检验,若红色石蕊试纸变蓝,说明有NH4+
.(7)将Y溶液滴入沸水可得到红褐色液体,反应的离子方程式是:
Fe3++3H2O
Fe(OH)3(胶体)+3H+
| ||
Fe3++3H2O
Fe(OH)3(胶体)+3H+
,此液体具有的性质是
| ||
abc
abc
(填写序号字母).a.光束通过该液体时形成光亮的“通路”
b.插入电极通直流电后,有一极附近液体颜色加深
c.向该液体中加入稀硫酸溶液,先有沉淀产生,后沉淀溶解
d.将该液体加热、蒸干、灼烧后,有氢氧化物生成.
分析:B、F为固态单质,其余为化合物,B呈黄色,则B为S,F为Fe,E为FeS,X应为H2SO4,所以H为FeCl2,G是气体,G为H2S,反应①为硫酸亚铁与氯气的反应,生成氯化铁和硫酸铁,所以Y、W的阳离子相同,均含有Fe3+,反应②为硫酸亚铁与硫化氢反应,生成B(S)、X(H2SO4)、H(FeSO4);D与碱反应生成Z,能发生连续氧化,则Z为NH3,D为(NH4)2SO4,I为NO,J为NO2,C为气体,C应为SO2,反应④为二氧化硫、二氧化氮在水中反应生成X(硫酸)和I(NO),由两种正盐组成的混合物A,与硫酸反应生成S、SO2、(NH4)2SO4,则A为(NH4)2S、(NH4)2SO3,然后结合物质的性质来解答.
解答:解:B、F为固态单质,其余为化合物,B呈黄色,则B为S,F为Fe,E为FeS,X应为H2SO4,所以H为FeCl2,G是气体,G为H2S,反应①为硫酸亚铁与氯气的反应,生成氯化铁和硫酸铁,所以Y、W的阳离子相同,均含有Fe3+,反应②为硫酸亚铁与硫化氢反应,生成B(S)、X(H2SO4)、H(FeSO4);D与碱反应生成Z,能发生连续氧化,则Z为NH3,D为(NH4)2SO4,I为NO,J为NO2,C为气体,C应为SO2,反应④为二氧化硫、二氧化氮在水中反应生成X(硫酸)和I(NO),由两种正盐组成的混合物A,与硫酸反应生成S、SO2、(NH4)2SO4,则A为(NH4)2S、(NH4)2SO3,
(1)A为(NH4)2S、(NH4)2SO3,故答案为:(NH4)2S;(NH4)2SO3;
(2)反应①为硫酸亚铁与氯气的反应,离子反应为2Fe2++Cl2=2Fe3++2Cl-,故答案为:2Fe2++Cl2=2Fe3++2Cl-;
(3)反应②为硫酸亚铁与硫化氢反应,离子反应为2Fe3++H2S=S↓+2Fe2++2H+,故答案为:2Fe3++H2S=S↓+2Fe2++2H+;
(4)反应③为氨气的催化氧化反应,该反应为4NH3+5O2
4NO+6H2O,故答案为:4NH3+5O2
4NO+6H2O;
(5)反应④为二氧化硫、二氧化氮在水中反应生成X(硫酸)和I(NO),该反应为NO2+SO2+H2O=H2SO4+NO,故答案为:NO2+SO2+H2O=H2SO4+NO;
(6)D中阳离子为铵根离子,取样品D于试管中,加入NaOH溶液,加热.用湿润的红色石蕊试纸在试管口检验,若红色石蕊试纸变蓝,说明有NH4+,
故答案为:取样品D于试管中,加入NaOH溶液,加热.用湿润的红色石蕊试纸在试管口检验,若红色石蕊试纸变蓝,说明有NH4+;
(7)Y溶液滴入沸水可得到红褐色液体,发生Fe3++3H2O
Fe(OH)3(胶体)+3H+,生成胶体,具有丁达尔现象、电泳、聚沉的性质,而将该液体加热、蒸干、灼烧后,最终为氧化铁,则选abc,故答案为:Fe3++3H2O
Fe(OH)3(胶体)+3H+;abc.
(1)A为(NH4)2S、(NH4)2SO3,故答案为:(NH4)2S;(NH4)2SO3;
(2)反应①为硫酸亚铁与氯气的反应,离子反应为2Fe2++Cl2=2Fe3++2Cl-,故答案为:2Fe2++Cl2=2Fe3++2Cl-;
(3)反应②为硫酸亚铁与硫化氢反应,离子反应为2Fe3++H2S=S↓+2Fe2++2H+,故答案为:2Fe3++H2S=S↓+2Fe2++2H+;
(4)反应③为氨气的催化氧化反应,该反应为4NH3+5O2
| ||
| ||
(5)反应④为二氧化硫、二氧化氮在水中反应生成X(硫酸)和I(NO),该反应为NO2+SO2+H2O=H2SO4+NO,故答案为:NO2+SO2+H2O=H2SO4+NO;
(6)D中阳离子为铵根离子,取样品D于试管中,加入NaOH溶液,加热.用湿润的红色石蕊试纸在试管口检验,若红色石蕊试纸变蓝,说明有NH4+,
故答案为:取样品D于试管中,加入NaOH溶液,加热.用湿润的红色石蕊试纸在试管口检验,若红色石蕊试纸变蓝,说明有NH4+;
(7)Y溶液滴入沸水可得到红褐色液体,发生Fe3++3H2O
| ||
| ||
点评:本题考查无机物的推断,明确物质的状态和颜色确定S、Fe为突破口,再结合反应②③推断出各物质是解答本题的关键,注意X为硫酸而不是盐酸为解答的难点,题目难度较大.

练习册系列答案
相关题目
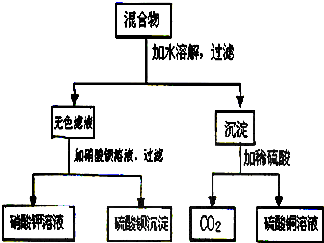 由A和B两种正盐组成的混合物,进行了下列实验:
由A和B两种正盐组成的混合物,进行了下列实验: