题目内容
下列物品所用材料为硅酸盐的是
| A.水晶镜片 | B.陶瓷餐具 | C.石英光导纤维 | D.计算机芯片 |
B
解析试题分析:A.水晶镜片的材料是水晶——二氧化硅。错误。B陶瓷餐具是以硅酸盐为材料制成的产品。正确。C.石英光导纤维主要材料是二氧化硅,不是硅酸盐。错误;D计算机芯片是高纯度的硅单质,不是以硅酸盐为材料错误。
考点:考查各种含硅的单质及化合物的应用的知识。

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
下列表述正确的是
①浓硝酸通常保存在棕色试剂瓶中
②检验亚硫酸钠溶液在空气中放置是否变质可以先加硝酸溶液,再加氯化钡溶液来检验
③锌与稀硝酸反应可以得到氢气
④足量铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化Fe2+
⑤ 浓硫酸滴到纸张上变黑,说明浓硫酸具有吸水性
⑥二氧化硫和二氧化氮都能形成酸雨,酸雨的pH等于5.6
| A.①③④ | B.①② | C.① | D.①②⑤⑥ |
下列由相关实验现象所推出的结论正确的是
| A.Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性 |
| B.向溶液中滴加酸化的Ba(NO3)2溶液出现白色沉淀,说明该溶液中一定有SO42- |
| C.Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应 |
| D.分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水 |
实验室制取少量干燥的氨气涉及下列装置,其中正确的是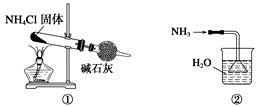
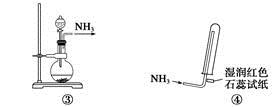
| A.①是氨气发生装置 | B.③是氨气发生装置 |
| C.②是氨气吸收装置 | D.④是氨气收集、检验装置 |
下列制取硫酸铜的实验设计中,能体现“经济、高效、环保”精神的最佳方案是( )。
| A.铜与浓硫酸共热 |
| B.用铜片为阳极,石墨为阴极,电解稀硫酸 |
| C.先灼烧废铜屑生成氧化铜,然后再用浓硫酸溶解 |
| D.适当温度下,使铜片在持续通入空气的稀硫酸中溶解 |
有a、b、c、d、e五种气体,现进行下列实验:
| (1)a和b混合 | 气体变红棕色 |
| (2)c和d混合 | 产生白烟 |
| (3)c和e分别通入少量溴水中 | 溴水都变成无色透明的液体 |
| (4)b和e分别通入氢硫酸中 | 都产生淡黄色浑浊 |
则a、b、c、d、e依次可能是( )
A.O2、NO、HCl、NH3、CO2
B.O2、NO、NH3、HCl、SO3
C.NO、O2、NH3、HCl、SO2
D.HCl、CO2、NH3、H2S、CH4
下列说法正确的是( )
| A.SO2和SO3都是酸性氧化物,二者的水溶液都是强酸 |
| B.将铜片放入浓硫酸中,无明显现象是因为铜片发生了钝化 |
| C.硫粉在过量的纯氧中燃烧可以生成大量的SO3 |
| D.富含硫黄的矿物在工业上可用于制造硫酸 |
烧瓶中放入铜片和稀硝酸,用酒精灯加热来制取较纯净的一氧化氮,反应开始后发现烧瓶中充满红棕色气体,这时的操作应是( )
| A.立即接收集容器,用向上排空气法收集 |
| B.待烧瓶中红棕色气体消失后,用向上排空气法收集 |
| C.待烧瓶中红棕色气体消失后,用排水法收集 |
| D.立即用排水法收集 |
在氯水中存在着如下反应:Cl2+H2O=HCl+HClO,因此氯水中存在多种分子和离子。在下列实验现象中与相应离子或分子性质关系正确的是( )
| A.氯水有刺激性气味说明氯水中有HCl |
| B.氯水中滴入品红溶液,溶液为无色说明氯水中有Cl2 |
| C.向氯水中通入SO2气体,氯水黄绿色褪去说明Cl2发生了反应 |
| D.向氯水中加入CaCO3有气泡产生,说明有HCl和HClO |