题目内容
在容积一定的密闭容器中,可逆反应A(g)+B(g)?xC(g),有如图所示的关系曲线,根据下图下列判断正确的是( )


分析:由图(Ⅰ)中a、b的相对位置知,增压(因p2>p1),w(C)升高,故x=1;由b、c的相对位置知,升温(因为T1>T2),w(C)降低.故正反应为放热反应.
即该反应为:A(g)+B(g) C(g)(正反应为放热反应),由反应式可知,升温和降压均可使反应向逆反应方向移动.
C(g)(正反应为放热反应),由反应式可知,升温和降压均可使反应向逆反应方向移动.
由图Ⅱ,y随温度的升高而降低,可判断y为A的转化率或混合气体的平均摩尔质量等量,结合压强对平衡移动的影响判断P3、P4的关系.
即该反应为:A(g)+B(g)
 C(g)(正反应为放热反应),由反应式可知,升温和降压均可使反应向逆反应方向移动.
C(g)(正反应为放热反应),由反应式可知,升温和降压均可使反应向逆反应方向移动.由图Ⅱ,y随温度的升高而降低,可判断y为A的转化率或混合气体的平均摩尔质量等量,结合压强对平衡移动的影响判断P3、P4的关系.
解答:解:依据图(Ⅰ)中a、b的相对位置知,增压(因p2>p1),w(C)升高,故x=1;
由b、c的相对位置知,升温(因为T1>T2),w(C)降低,故正反应为放热反应.
即该反应为:A(g)+B(g) C(g)(正反应为放热反应),由反应式可知,升温和降压均可使反应向逆反应方向移动.
C(g)(正反应为放热反应),由反应式可知,升温和降压均可使反应向逆反应方向移动.
由图(Ⅱ)知:因升温y降低,故y降低的方向必为压强减小的方向,所以,P3>P4,随着温度的升高,平衡将向左移动,A的转化率降低;随着压强的减小,A物质的转化率减小,
只有A符合P3>P4,
故选A.
由b、c的相对位置知,升温(因为T1>T2),w(C)降低,故正反应为放热反应.
即该反应为:A(g)+B(g)
 C(g)(正反应为放热反应),由反应式可知,升温和降压均可使反应向逆反应方向移动.
C(g)(正反应为放热反应),由反应式可知,升温和降压均可使反应向逆反应方向移动.由图(Ⅱ)知:因升温y降低,故y降低的方向必为压强减小的方向,所以,P3>P4,随着温度的升高,平衡将向左移动,A的转化率降低;随着压强的减小,A物质的转化率减小,
只有A符合P3>P4,
故选A.
点评:本题旨在考查学生对化学平衡图象的理解.解答这类图象题,首先要“译”出其化学含义.由于勒夏特列原理只适用于“单因素”(浓度或温度或压强)改变,分析时应固定一个物理量,分析另一物理量对纵坐标的影响.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
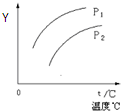 (2010?淮南一模)在容积一定的密闭容器中发生可逆反应A(g)+2B(g)?2C(g);△H>0,平衡移动关系如图所示.下列说法正确的是( )
(2010?淮南一模)在容积一定的密闭容器中发生可逆反应A(g)+2B(g)?2C(g);△H>0,平衡移动关系如图所示.下列说法正确的是( ) 在容积一定的密闭容器中,可逆反应:A2 (g)+B2(g)?nC(g)符合图Ⅰ所示关系.由此推断,对图Ⅱ的说法不正确的是( )
在容积一定的密闭容器中,可逆反应:A2 (g)+B2(g)?nC(g)符合图Ⅰ所示关系.由此推断,对图Ⅱ的说法不正确的是( )