题目内容
掌握仪器的名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。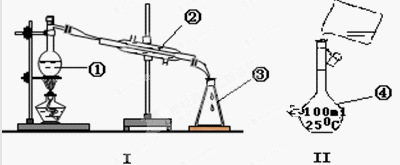
⑴写出下列仪器的名称:
①____________;②_____________;④__________;
⑵仪器①~④中,使用时必须检查是否漏水的有______。(填序号)
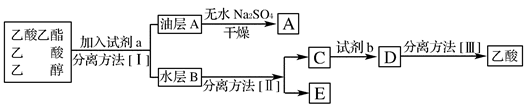
⑶若利用装置I分离四氯化碳和乙醇的混合物,还缺少的仪器是_________,将仪器补充完整后进行的实验操作的名称为_____________ 。现需配制250 mL 0.2 mol/L NaCl溶液,装置II是某同学转移溶液的示意图,图中的错误是______________、_________________ 。
(8分)(1)蒸馏烧瓶;冷凝管;容量瓶(2分)
(2)④(2分)(3)温度计;(2分)分馏;(2分)
未用玻璃棒引流;(2分)未采用250ml容量瓶(各2分)
解析试题分析:(1)蒸馏烧瓶;冷凝管;容量瓶
(2)容量瓶是用来精确配置一定体积一定浓度物质的量浓度溶液的仪器,如果漏水,再定容后摇匀要有液体流出,这种情况下如果你的液体没有摇匀,会造成溶剂减少,或溶质减少造成配置的溶液浓度偏大或偏小,当然如果不用摇匀你的溶液就是均匀的,那么浓度就不会改变,只是体积减少点。但这种情况很少吧,所以为了保证浓度,一定要检验是否漏水。
(3)因为四氯化碳和乙醇互溶且沸点不同,所以利用这二者的沸点不同的原理(乙醇的沸点比较低)来进行分离,所以需要温度计进行测量,这种利用二者的沸点不同进行分离的办法叫做蒸馏;
未用玻璃棒引流;未采用250ml容量瓶
考点:本题着重考查定容实验。

 阅读快车系列答案
阅读快车系列答案实验室可用K2Cr2O7固体与浓盐酸混合加热制备氯气(K2Cr2O7被还原为Cr3+)。
(1)K2Cr2O7与浓盐酸反应的化学方程式为_______;若反应中转移3 mol e-,则消耗_______mol K2Cr2O7
(2)稀盐酸与K2Cr2O7固体混合加热没有氯气生成。为探究影响氯气生成的因素,某化学兴趣小组进行如下实验:
①提出假设
假设1:Cl-浓度对反应有影响;
假设2:H+浓度对反应有影响;
假设3: _____________________。
②设计实验方案,进行实验。写出实验步骤及预期现象和结论。
限选举实验试剂:浓盐酸、稀盐酸、浓硫酸、NaOH溶液、K2Cr2O7固体、NaCl固体、湿润的淀粉KI试纸
| 实验步骤 | 预期现象和结论 |
| 步:1:向盛有K2Cr2O7固体的A、B两试管中分别加入一定量的稀盐酸。 | |
| 步骤2: | |
| 步骤3: | |
实验室常利用甲醛(HCHO)法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH4+ +6HCHO =3H++6H2O+(CH2)6N4H+ [滴定时,1 mol (CH2)6N4H+与 l mol H+相当,然后用NaOH标准溶液滴定反应生成的酸。某兴趣小组用甲醛法进行了如下实验:
步骤I 称取样品1.500 g。
步骤II 将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤III 移取25.00 mL样品溶液于250 mL锥形瓶中,加入10 mL 20%的中性甲醛溶液,摇匀、静置5 min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
(1)根据步骤III填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数________(填“偏高”、“偏低”或“无影响”)。
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积_______(填“偏大”、“偏小”或“无影响”)
③滴定时边滴边摇动锥形瓶,眼睛应观察____________。
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
④滴定达到终点时现象:__________________________________________________。
(2)滴定结果如下表所示:
| 滴定 次数 | 待测溶液的体积 /mL | 标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
若NaOH标准溶液的浓度为0.1010 mol·L-1,则该样品中氮的质量分数为___________。
铁是人体不可缺少的微量元素,摄入含铁的化合物可补充铁。“速力菲”是市场上一种常见的补铁药品,下表是说明书的部分内容。
[规格]每片含琥珀酸亚铁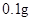 [适应症]用于缺铁性贫血症,预防及治疗用。 [用量用法]成人预防量 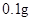 /日,成人治疗量 /日,成人治疗量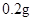 — —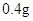 /日。 /日。小儿用量预防量 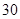 — —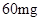 /日,治疗量 /日,治疗量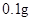 — —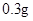 /日 /日[贮藏]避光、密封、在干燥处保存。 |
(1)该药品中Fe2+会缓慢氧化。国家规定该药物中Fe2+的氧化率(已经被氧化Fe2+的质量与Fe2+总质量的比值)超过10.00% 即不能再服用。
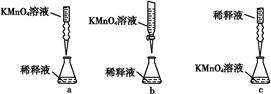
①实验室可采用H2SO4酸化的KMnO4溶液,对“速力菲”中的Fe2+进行滴定(假设药品中其他成份不与KMnO4反应)。请写出该反应的离子方程式: 。
②实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的玻璃仪器除玻璃棒、烧杯、胶头滴管外,还需 。
③某同学设计了下列滴定方式(夹持部分略去),最合理的是 。(填字母序号)
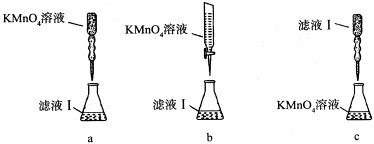
(2)称量上述含铁元素质量分数为20.00%的“速力菲”10.00 g,将其全部溶于稀H2SO4中,配制成1000 ml溶液,取出20.00 ml,用0.01000 mol?L-1的KMnO4溶液滴定,用去KMnO4溶液12.00 ml ,该药品中Fe2+的氧化率为 。
(3)已知琥珀酸为二元有机羧酸,含23.6 g琥珀酸的溶液与4.0 mol?L-1 100.0 ml的氢氧化钠溶液恰好完全中和。核磁共振氢谱分析显示,琥珀酸分子谱图上只有两组吸收峰。写出琥珀酸溶液与氢氧化钠溶液完全中和的化学方程式(有机物写结构简式) 。
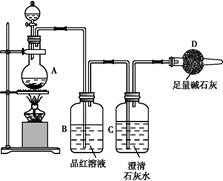
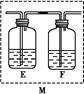
下图是用实验室制得的乙烯(C2H5OH  CH2=CH2↑+H2O)与溴水作用制取1,2-二溴乙烷的部分装置图,根据图示判断下列说法正确的是( )
CH2=CH2↑+H2O)与溴水作用制取1,2-二溴乙烷的部分装置图,根据图示判断下列说法正确的是( )
| A.装置①和装置③中都盛有水,其作用相同 |
| B.装置②和装置④中都盛有NaOH溶液,其吸收的杂质相同 |
| C.产物可用分液的方法进行分离,1,2-二溴乙烷应从分液漏斗的上口倒出 |
| D.制备乙烯和生成1,2-二溴乙烷的反应类型分别是消去反应和加成反应 |
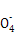 +8H+
+8H+ 5Fe3++Mn2++4H2O)。
5Fe3++Mn2++4H2O)。