题目内容
5.某有机物链状分子中含n个-CH2-,m个 ,a个-CH3,其余为-Cl.则该有机物分子中Cl的个数为( )
,a个-CH3,其余为-Cl.则该有机物分子中Cl的个数为( )| A. | m+n+a | B. | m+2-a | C. | 2n+3m-a | D. | m+2n+2-a |
分析 该有机物中含有a个甲基,n个亚甲基(-CH2-),m个次甲基(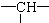 ),其余为氯原子,说明该物质属于饱和氯代烃,将Cl原子换为H原子就是烷烃结构,根据烷烃通式计算出H原子个数,计算已知的H原子个数,剩余的就是Cl原子个数,据此分析解答.
),其余为氯原子,说明该物质属于饱和氯代烃,将Cl原子换为H原子就是烷烃结构,根据烷烃通式计算出H原子个数,计算已知的H原子个数,剩余的就是Cl原子个数,据此分析解答.
解答 解:某有机物链状分子中含a个甲基,n个亚甲基(-CH2-),m个次甲基(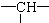 ),其余为氯原子,说明该物质属于饱和氯代烃,将Cl原子换为H原子就是烷烃结构,该分子中C原子个数=(a+n+m),根据烷烃通式知H原子个数=2(a+n+m)+2,a个甲基、n个亚甲基(-CH2-)、m个次甲基(
),其余为氯原子,说明该物质属于饱和氯代烃,将Cl原子换为H原子就是烷烃结构,该分子中C原子个数=(a+n+m),根据烷烃通式知H原子个数=2(a+n+m)+2,a个甲基、n个亚甲基(-CH2-)、m个次甲基(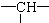 )中H原子总数=3a+2n+m,则缺少的H原子个数=2(a+n+m)+2-(3a+2n+m)=m+2-a,所以氯原子个数为m+2-a,
)中H原子总数=3a+2n+m,则缺少的H原子个数=2(a+n+m)+2-(3a+2n+m)=m+2-a,所以氯原子个数为m+2-a,
故选B.
点评 本题考查常见有机物结构,侧重考查学生知识迁移能力,采用补缺法分析解答即可,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.设NA表示阿伏加德罗常数的数值,下列叙述中正确的是( )
| A. | 0.5 mol锌粒与足量盐酸反应产生11.2 L H2 | |
| B. | 标准状况下,18g的H2O中含有的电子数为10NA | |
| C. | 常温常压下,11.2L氧气所含的原子数为NA | |
| D. | 2.4g金属镁变为镁离子失去的电子数为0.1NA |
16.FeCl3、CuCl2混溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的( )
| A. | 加入KSCN的溶液一定不变红色 | B. | 溶液中一定含有Fe3+ | ||
| C. | 溶液中可能含Cu2+ | D. | 剩余固体中一定有铜 |
13.0.25L 1mol/L FeCl2溶液中的Cl-的物质的量浓度为( )
| A. | 1 mol/L | B. | 1.5 mol/L | C. | 2mol/L | D. | 3 mol/L |
20.下列说法正确的是( )
| A. | H2SO4电离方程式H2SO4=2H++S6++4O2- | |
| B. | H2、D2、T2互为同位素 | |
| C. | 18g H2O含有的电子数为10NA | |
| D. | ${\;}_{62}^{144}$Sm与${\;}_{62}^{150}$Sm的核外电子数和中子数均为62 |
10.若用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 0.1 mol Cl2与足量的铁粉完全反应,转移的电子数为0.2NA | |
| B. | 2.3gNa与水完全反应生成H21.12L | |
| C. | NA个氧原子的质量约为32g | |
| D. | 标准状况下,2.24L CCl4含有的CCl4分子数为0.1NA |
17.相同物质的量的下列有机物,充分燃烧,消耗氧气量相同的是( )
| A. | C3H4和C3H6O | B. | C3H6和C3H8O2 | C. | C3H6O2和C3H8O | D. | C3H8O和C4H6O |
14.下列说法正确的是( )
| A. | 江河入海口三角洲的形成通常与胶体的性质有关 | |
| B. | 煤的干馏和石油的分馏均属化学变化 | |
| C. | BaSO4在医学上用作钡餐,Ba2+对人体无毒 | |
| D. | 14C可用于文物的年代鉴定,12C与14C互为同素异形体. |
2.下列说法正确的是( )
| A. | 某溶液与NaOH 溶液共热,产生使湿润的红色石蕊试纸变蓝色的气体,说明原溶液中存在NH4+ | |
| B. | 某溶液中加入AgNO3 溶液时,产生白色沉淀,说明原溶液中一定存在Cl- | |
| C. | 某溶液中滴加BaCl2 溶液时,产生白色沉淀,说明原溶液中一定存在SO42- | |
| D. | 焰色反应中火焰显黄色,说明样品中存在钠元素,不存在钾元素 |