题目内容
将一定体积的稀硝酸溶液平均分成两份,一份与足量的铜粉反应收集到气体的体积V1 ,另一份先加入与其等体积的稀硫酸,再投入足量的铜粉收集到的气体的体积为V2 (V1与V2都是在同一条件下测定)。已测得2 V1=V2,则稀硝酸与稀硫酸的物质的量浓度之比为
| A.1:1 | B.3:1 | C.2:1 | D.任意比 |
C
设每份硝酸中硝酸的物质的量为a mol
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
第一份硝酸中产生的NO的物质的量为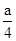 mol(H+全部参加反应,可由其计算)
mol(H+全部参加反应,可由其计算)
第二份硝酸由硫酸补充了部分H+,如果溶液中的NO3-全部被还原,则可得到NO为a mol,不符合题意,故NO3-没有全部参加反应;
设硫酸溶液中硫酸的物质的量为b mol,溶液中H+共(a+2b)mol,可得到NO为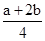 mol
mol
由题意知: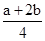 =2×
=2×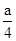 ,即a=2b
,即a=2b
由于两溶液等体积,故硝酸的浓度硫酸的两倍,答案为C
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
第一份硝酸中产生的NO的物质的量为
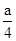 mol(H+全部参加反应,可由其计算)
mol(H+全部参加反应,可由其计算)第二份硝酸由硫酸补充了部分H+,如果溶液中的NO3-全部被还原,则可得到NO为a mol,不符合题意,故NO3-没有全部参加反应;
设硫酸溶液中硫酸的物质的量为b mol,溶液中H+共(a+2b)mol,可得到NO为
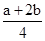 mol
mol由题意知:
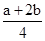 =2×
=2×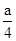 ,即a=2b
,即a=2b由于两溶液等体积,故硝酸的浓度硫酸的两倍,答案为C

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
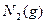 +
+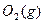 青
青 2
2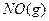 ;
;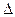 H=180.74KJ/mol.此反应称为伯克莱特—艾,某次雷雨闪电中两块云间的电势差为1×
H=180.74KJ/mol.此反应称为伯克莱特—艾,某次雷雨闪电中两块云间的电势差为1×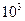 V,从一块云移到另一块云的电荷量为30000C,此次闪电释放出的能量为 KJ .
V,从一块云移到另一块云的电荷量为30000C,此次闪电释放出的能量为 KJ . 混合气体在标准状况下的体积为5.6L。请回答:
混合气体在标准状况下的体积为5.6L。请回答: 浓度。
浓度。