题目内容
【题目】短周期元素X、Y、Z、W在元素周期表中相对位置如图所示,其中Y所处的周期序数与族序数相等。按要求回答下列问题:
X | ||||
Y | Z | W |
(1)写出W的离子结构示意图__________
(2)比较W 与Z的最高价氧化物对应水化物酸性的强弱 (写化学式)
(3)写出X的氢化物的电子式 ,写出X氢化物的水溶液与X的最高价氧化物对应的水化物的水溶液反应的离子方程式
(4)已知:① C(s)+ O2(g)= CO2(g) ![]() H=a kJ· mol-1;② CO2(g) +C(s)=2CO(g)
H=a kJ· mol-1;② CO2(g) +C(s)=2CO(g) ![]() H=b kJ· mol-1;
H=b kJ· mol-1;
③ Si(s)+ O2(g)=SiO2(s) ![]() H=c kJ· mol-1。写出工业生产中用碳粉还原二氧化硅制取粗硅的热化学方_____________________________。
H=c kJ· mol-1。写出工业生产中用碳粉还原二氧化硅制取粗硅的热化学方_____________________________。
【答案】(1)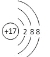
(2)HClO4 >H2SiO3
(3)![]() NH3·H2O + H+ = NH4+ + H2O
NH3·H2O + H+ = NH4+ + H2O
(4)2C(s) + SiO2(s) = Si(s) + 2CO(g) △H=(a+b-c)kJ·mol-1
【解析】根据元素在周期表中的位置,强判断Y是铝元素,Z是硅元素,X是氮元素,W是氯元素。
(1)写出W的离子结构示意图为 ;(2)非金属性Cl>Si,最高价氧化物对应水化物酸性:
;(2)非金属性Cl>Si,最高价氧化物对应水化物酸性:
HClO4 >H2SiO3;(3)氨气的电子式为:![]() ,氨水和硝酸反应的离子方程式为:NH3·H2O + H+ = NH4+ + H2O;(4)由盖斯定律,①+②-③可得:2C(s) +SiO2(s) = Si(s) + 2CO(g) △H=(a+b-c)kJ·mol-1。
,氨水和硝酸反应的离子方程式为:NH3·H2O + H+ = NH4+ + H2O;(4)由盖斯定律,①+②-③可得:2C(s) +SiO2(s) = Si(s) + 2CO(g) △H=(a+b-c)kJ·mol-1。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目