题目内容
(12分)已知某二元酸(化学式用H2RO4表示)在水中的电离方程式为:
H2RO4=H++HRO4-;HRO4 H++ RO42-回答下列问题:
H++ RO42-回答下列问题:
(1)NaHRO4溶液显 (填“酸性”、“中性”或“碱性”),理由是?
(用离子方程式和必要的文字说明)。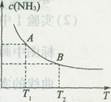
(2)Na2RO4溶液湿 (填“酸性”、“中性”或“碱性”),理由是?
(用离子方程式表示)
(3)如果25℃时,0.1 mol/L的NaHRO4溶液中,c(RO42-)=0.029 moL/L,则0.1mol/L H2RO4溶液中c(RO42-) 0.029 mol/L(填“<”、“>”或“=”),理由是 。
(4)25℃时,0.1 mol/L的NaHR04溶液中,各离子浓度由大到小的顺序是 。
(1) 酸性 (1分) HRO4—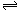 H++RO42—且HRO4—不水解(2分)
H++RO42—且HRO4—不水解(2分)
(2) 碱性(1分) RO42—+H2O 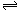 HRO4—+OH— (2分)
HRO4—+OH— (2分)
(3) < (2分) H2RO4第一步电离产生的H+抑制了第二步电离(2分)
(4) c(Na+) >c(HRO4—)>c(H+)>c(RO42-)>c(OH—) (2分)
解析

练习册系列答案
相关题目
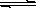 H++HA-, HA-
H++HA-, HA- H++HA-,
HA-
H++HA-,
HA-