题目内容
(10分)下表为元素周期表中的一部分.用化学式或元素符号回答下列问题:
(1)10种元素中,化学性质最不活泼的是__________(填元素名称)。
(2)在①②⑤的最高价氧化物的水化物中,碱性最强的是__________(填化学式)。
(3)元素⑦的常见的氢化物的化学式为__ __,该氢化物常温下和元素②的单质反应的离子方程式是:_______________________,该氢化物与元素⑧的单质反应的离子方程式是___________________________。
(4)①和⑨的最高价氧化物对应的水化物化学式分别为___________和_______。
(5)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为__________________
(6)⑧与⑨分别与H2形成的氢化物的稳定性:__________,(用化学式表示)最高价氧化物对应的水溶液的酸性:_______________。(用化学式)
| | IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 2 | | | | ⑥ | | ⑦ | | |
| 3 | ① | ③ | ⑤ | | | | ⑧ | ⑩ |
| 4 | ② | ④ | | | | | ⑨ | |
(2)在①②⑤的最高价氧化物的水化物中,碱性最强的是__________(填化学式)。
(3)元素⑦的常见的氢化物的化学式为__ __,该氢化物常温下和元素②的单质反应的离子方程式是:_______________________,该氢化物与元素⑧的单质反应的离子方程式是___________________________。
(4)①和⑨的最高价氧化物对应的水化物化学式分别为___________和_______。
(5)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为__________________
(6)⑧与⑨分别与H2形成的氢化物的稳定性:__________,(用化学式表示)最高价氧化物对应的水溶液的酸性:_______________。(用化学式)
(1)氩(2)KOH(3)H2O;2K+2H2O==2K++2OH―+H2↑;Cl2+H2O H++Cl―+HClO
H++Cl―+HClO
NaOH;HBrO4 (5)NaOH+Al(OH)3==NaAlO2+2H2O
(6) HCl>HBr;HClO4>HBrO4
 H++Cl―+HClO
H++Cl―+HClONaOH;HBrO4 (5)NaOH+Al(OH)3==NaAlO2+2H2O
(6) HCl>HBr;HClO4>HBrO4
试题分析:(1)零族元素最外层达到了稳定结构,化学性质稳定;(2)同主族最高价氧化物对应水化物碱性逐渐增强,同周期最高价氧化物对应水化物碱性逐渐减弱,故KOH>NaOH>Al(OH)3;(3)元素⑦为O,故氢化物为H2O;钾和水反应生成氢氧化钾和氢气;元素⑧为氯,氯气和水反应生成盐酸和次氯酸,次氯酸是弱酸,不能写成离子形式;(4)①为钠,钠的最高价氧化物对应的水化物为NaOH,⑨为溴,溴的最高价氧化物对应水化物为高溴酸,即HBrO4;(5)氢氧化钠和氢氧化铝反应的方程式;(6)同主族气态氢化物的稳定性逐渐减弱,故HCl>HBr,最高价氧化物对应水化物的酸性逐渐减弱,故HClO4>HBrO4

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目

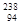 Pu作为热源材料。下列关于
Pu作为热源材料。下列关于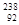 U互为同位素
U互为同位素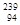 Pu互为同素异形体
Pu互为同素异形体