题目内容
【题目】如图所示是425℃时,在1 L密闭容器中发生化学反应的浓度随时间的变化示意图。
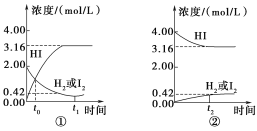
下列叙述错误的是( )
A. 图①中t0时,三种物质的物质的量相同
B. 图①中t0时,反应达到平衡状态
C. 图②中的可逆反应为2HI(g) ![]() H2(g)+I2(g)
H2(g)+I2(g)
D. 图①②中当c(HI)=3.16 mol/L时,反应达到平衡状态
【答案】B
【解析】
A.图①中t0时,由图可知三种物质的物质的量浓度相等,由于体系恒容,所以三者的物质的量也相等,故A正确;
B.图①中t0时,由图可知三种物质的物质的量浓度相等,但t0后各物质的量浓度未保持不变,反应没有达到平衡状态,故B错误;
C.由图②可知,该图表示的反应为2HI(g)=H2(g)+I2(g)。该反应可达平衡状态,所以图②的逆反应为H2(g)+I2(g)=2HI(g),故C正确;
D.由图可知:图①、②中当c(HI)=3. 16mol/L时,之后各物质的物质的量浓度都保持不变,说明反应均达到平衡状态,故D正确;
故选B。

 名校课堂系列答案
名校课堂系列答案【题目】A、B、C、D、E是五种短周期元素。已知:它们的原子序数依次增大,A是元素周期表中原子半径最小的元素;B原子最外层电子数比其次外层电子数多2,C是E的邻族元素;D和E的原子序数之和为30,且D的族序数与周期数相等。甲、乙、丙、丁是它们两两形成的化合物,其中甲分子中含有18个电子。
物质组成 | 甲 | 乙 | 丙 | 丁 |
化合物中各元素 原子个数比 | A和C 1:1 | B和A 1:4 | D和E 1:3 | B和E 1:4 |
请回答下列问题:
(1)元素E在周期表中的位置为___________________________;
(2)把D的单质放到NaOH溶液中,反应的化学方程式为:_______________________;
(3)用电子式表示甲的形成过程:_________________________;
(4)在密闭容器中充入BC2、BC和乙的混合气体共mg,若加入足量Na2O2,充分振荡并不断用电火花点燃至反应完全,测得固体质量增重mg,则BC2与乙的体积比为________________;
(5)有200mL MgCl2和丙的混合溶液,其中c(Mg2+)= 0.2 mol· L-1,c(Cl-)= 1.3mol·L-1,要使Mg2+全部转化为沉淀分离出来,至少需要4 mol·L-1 NaOH 溶液的体积是:______。
