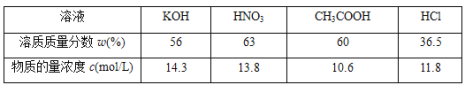
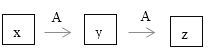
题目内容
【题目】某合金X由常见的两种元素组成。为探究该合金X的元素组成和性质,设计并进行如下实验:
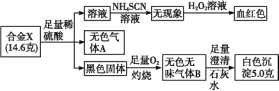
根据上述信息,回答下列问题:
(1)合金X的化学式为________。
(2)用离子方程式解释溶液中滴加H2O2后呈红色的原因:_______
(3)写出336 mL(标准状况)气体B通入100 mL 0.2 mol/L 的NaOH溶液中的化学反应方程式:_______
【答案】Fe5C H2O2+2H++2Fe2+=2Fe3++2H2O、Fe3++3SCN-=Fe(SCN)3 4NaOH+3CO2=Na2CO3+2NaHCO3+H2O
【解析】
由血红色可以推出X含有铁元素,由无色无味的气体使澄清石灰水变浑浊推出X中另一种元素为碳。铁碳合金和足量的稀硫酸反应生成FeSO4和H2(A气体),剩余黑色固体碳在足量的氧气中灼烧,生成无色无味气体B(CO2),CO2通入足量澄清石灰水中得到白色沉淀CaCO3。
(1)生成的CaCO3为5.0 g即0.05 mol,碳元素的质量为0.05 mol×12 g/mol=0.6 g,则X中铁的含量为14.6 g-0.6 g=14.0 g,即含铁14.0g÷56g/mol=0.25 mol,所以X为Fe5C。
(2)合金中的Fe与H2SO4反应生成的是FeSO4,加氧化剂H2O2后被氧化成Fe3+再与SCN-生成Fe(SCN)3。故离子方程式为:H2O2+2H++2Fe2+=2Fe3++2H2O、Fe3++3SCN-=Fe(SCN)3;
(3)CO2的物质的量为0.336L÷22.4L/mol=0.015 mol,NaOH的物质的量为0.02mol。0.015molCO2与0.02 mol NaOH反应生成Na2CO3 a mol与NaHCO3 b mol,根据Na和C守恒列2个二元一次方程分别为2a+b=0.02,a+b=0.015解得a=0.005,b=0.01,根据四种物质的最简比写出方程式:4NaOH+3CO2=Na2CO3+2NaHCO3+H2O。

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案【题目】阿司匹林(乙酰水杨酸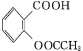 )是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135 ℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备的主要反应为
)是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135 ℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备的主要反应为
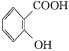 +(CH3CO)2O
+(CH3CO)2O![]()
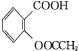 +CH3COOH
+CH3COOH
制备基本操作流程如下:
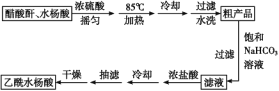
主要试剂和产品的物理常数:
名称 | 相对分子质量 | 熔点或沸点(℃) | 水 |
水杨酸 | 138 | 158(熔点) | 微溶 |
醋酸酐 | 102 | 139.4(沸点) | 反应 |
乙酰水杨酸 | 180 | 135(熔点) | 微溶 |
请根据以上信息回答下列问题:
(1)合成过程中最合适的加热方法是__________。
(2)提纯粗产品时加入饱和NaHCO3溶液至没有CO2产生为止,再过滤,则加饱和NaHCO3溶液的目的是______
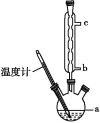
(3)另一种改进的提纯方法,称为重结晶提纯法。改进的提纯方法中加热回流的装置如图所示,仪器a的名称是____,冷凝管中冷凝水的进入口是____(填“b”或“c”),使用温度计的目的是_________
(4)检验产品中是否含有水杨酸的化学方法是_________
(5)该学习小组在实验中原料用量:2.76 g水杨酸、7.5 mL醋酸酐(ρ=1.08 g/cm3),最终称量产品m=2.92 g,则所得乙酰水杨酸的产率为____。