题目内容
关于阿伏加德罗常数(用NA表示)的下列叙述完全正确的是( )A.在标准状况下,密闭容器中11.2LNO与11.2LO2混合后气体分子数为0.75NA
B.由3个碳原子形成的有机化合物,1mol该物质最多含有的C-C单键数为2NA
C.在铜锌硫酸原电池中,当Cu极生成0.2gH2,则电路通过电子数为0.2NA
D.标准状况下,22.4L水中含分子数为NA
【答案】分析:A、根据反应2NO2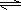 N2O4判断;
N2O4判断;
B、如是环丙烷,则含1个环丙烷分子中含有3个C-C单键;
C、根据化合价的变化和原电池正负极转移电子数目相等来判断;
D、根据标准状况下水的存在形式来判断.
解答:解:A、在标准状况下,密闭容器中11.2LNO与11.2LO2混合后生成11.2LNO2,剩余5.6LO2,但由于存在2NO2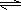 N2O4反应,则密闭容器中11.2LNO与11.2LO2混合后气体分子数小于
N2O4反应,则密闭容器中11.2LNO与11.2LO2混合后气体分子数小于
0.75NA,故A错误;
B、如是环丙烷,则含1个环丙烷分子中含有3个C-C单键,由3个碳原子形成的有机化合物,1mol该物质最多含有的C-C单键数为2NA或3NA,故B错误;
C、根据原电池正极反应为:2H++2e-═H2↑,0.2gH2的物质的量为0.1mol,所以转移的电子数为0.2NA,故C正确;
D、标准状况下水为液体,不是气体,无法确定物质的量,故D错误.
故选C.
点评:本题考查阿伏加德罗常数,题目难度不大,做题时注意物质存在的条件、状态以及物质的结构和性质等问题,审题是做好本题的关键.
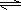 N2O4判断;
N2O4判断;B、如是环丙烷,则含1个环丙烷分子中含有3个C-C单键;
C、根据化合价的变化和原电池正负极转移电子数目相等来判断;
D、根据标准状况下水的存在形式来判断.
解答:解:A、在标准状况下,密闭容器中11.2LNO与11.2LO2混合后生成11.2LNO2,剩余5.6LO2,但由于存在2NO2
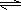 N2O4反应,则密闭容器中11.2LNO与11.2LO2混合后气体分子数小于
N2O4反应,则密闭容器中11.2LNO与11.2LO2混合后气体分子数小于0.75NA,故A错误;
B、如是环丙烷,则含1个环丙烷分子中含有3个C-C单键,由3个碳原子形成的有机化合物,1mol该物质最多含有的C-C单键数为2NA或3NA,故B错误;
C、根据原电池正极反应为:2H++2e-═H2↑,0.2gH2的物质的量为0.1mol,所以转移的电子数为0.2NA,故C正确;
D、标准状况下水为液体,不是气体,无法确定物质的量,故D错误.
故选C.
点评:本题考查阿伏加德罗常数,题目难度不大,做题时注意物质存在的条件、状态以及物质的结构和性质等问题,审题是做好本题的关键.

练习册系列答案
相关题目