题目内容
某学校的实验室有一瓶碳酸氢钠,由于放置时间过久,不知是否变质。
(1)请你利用所学过的知识,设计一个简单的实验,确定这瓶碳酸氢钠是否变质。你设计的实验方案:_____________________________________________。
(2)如果变质了,请你设计实验方案,确定其是否完全变质。你设计的实验方案:____________________________________________________________________________
________________________________________________________________________。
解析: NaHCO3易分解,如果NaHCO3中含有Na2CO3,说明NaHCO3已变质。鉴别NaHCO3中是否含有Na2CO3可用CaCl2溶液。若NaHCO3完全变质,就会全部生成Na2CO3。确定NaHCO3是否完全变质,可用加热法,若加热时有气体生成,且该气体使澄清石灰水变浑浊,说明没有完全变质,否则,说明完全变质。
答案: (1)取固体少量,加入试管中,加水配成溶液后滴加CaCl2溶液,若有白色沉淀生成,说明NaHCO3已变质,若无白色沉淀生成,说明NaHCO3没有变质
(2)取少量固体装入试管中,并塞上带有导管的单孔塞,将导管插入澄清石灰水中,加热,若有使澄清石灰水变浑浊的气体生成,说明没有完全变质。否则,说明已完全变质

 一线名师权威作业本系列答案
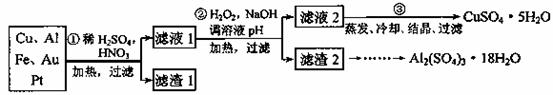
一线名师权威作业本系列答案某校化学小组的同学将一批废弃的线路板简单处理后,得到含Cu、Al、Fe及少量Au、Pt等金属的混合物,并设计了如下制备硫酸铜和硫酸铝晶体的方案:
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 2.2 | 3.2 |
| Al3+ | 3.7 | 4.7 |
| Cu 2+ | 5.6 | 6.4 |
回答下列问题:
①第①步参加反应的金属有 。
②第②步加入H2O2是因为滤液1中含有 离子。使用H2O2的优点是 。
③用第③步所得CuSO4·5H2O制备无水硫酸铜的方法是: 。
④请帮助化学小组的同学完成由滤渣2制取Al2(SO4) 3·18H2O 的实验步骤:
(1)取滤渣2,加入足量的 ,充分反应后过滤;
(2)取滤液,加入足量的 (填写试剂的化学式),然后过滤洗涤;
(3)用适量稀硫酸溶解;
(4)最后经过 (填写所需实验操作的名称),获得Al2(SO4)3·18H2O晶体。

 Y
Y W
W