题目内容
将a摩H2S和1摩O2置于一个容积可变的容器内进行反应.维持容器内气体的压强不变(101千帕),在120℃下测得反应前后容器内气体的密度分别为d1和d2.若a的取值不同,则H2S的氧化产物可能有如下三种情况:
(1)全部是SO2,此时a的取值范围是
(2)全部是S,此是a的取值范围是
(3)部分是SO2,部分是S,此时a的取值范围是
<a<2
<a<2.反应所生成的SO2的物质的量为
1+
摩.(以含a的代数式表示)
(1)全部是SO2,此时a的取值范围是
a≤
| 2 |
| 3 |
a≤
.| 2 |
| 3 |
(2)全部是S,此是a的取值范围是
a≥2
a≥2
,并且d1大于
大于
d2(填“小于“、“大于“或“等于“).(3)部分是SO2,部分是S,此时a的取值范围是
| 2 |
| 3 |
| 2 |
| 3 |
1-
| a |
| 2 |
1-
摩,容器内气体的物质的量之和为 | a |
| 2 |
1+
| a |
| 2 |
分析:所发生的反应为:2H2S+3O2=2SO2+2H2O(g),2H2S+O2=2S+2H2O(g)当
不同时,根据反应的数轴分析: .
.
| n(H2S) |
| n(O2) |
 .
.解答:解:反应为:2H2S+3O2=2SO2+2H2O(g) ①
2H2S+O2=2S+2H2O(g) ②
可由数轴分析:

(1)当全部为SO2时O2过量,或恰好发生反应①
即n(H2S):n(O2)=a:1≤2:3,a≤
,
故答案为:a≤
;
(2)当全部为S时,H2S过量,或恰好发生反应②
即n(H2S):n(O2)=a:1≥2:1 a≥2
又反应前后等压;密度比等于相对分子质量之比,反应前后气体相对分子质量都大于18,所以d1>d2.
故答案为:a≥2;大于;
(3)当SO2、S同时有时;①、②反应都发生,a取值必为
<a<2.
设反应过程是向a L H2S中逐渐通入O2,先发生反应②,O2未用完.所生成物量用H2S计算:即S=a mol,H2O=a mol,
耗O2=
mol,余O2=(1-
) mol,而过量O2可与S反应:S+O2═SO2 ③
由反应可知,生成n(SO2)=n(O2)=(1-
) mol.
反应生成气体总量为n(SO2)+n(H2O)=1-
+a=(1+
) mol
故答案为:
<a<2;1-
;1+
.
2H2S+O2=2S+2H2O(g) ②
可由数轴分析:
| n(H2S) |
| n(O2) |

(1)当全部为SO2时O2过量,或恰好发生反应①
即n(H2S):n(O2)=a:1≤2:3,a≤
| 2 |
| 3 |
故答案为:a≤
| 2 |
| 3 |
(2)当全部为S时,H2S过量,或恰好发生反应②
即n(H2S):n(O2)=a:1≥2:1 a≥2
又反应前后等压;密度比等于相对分子质量之比,反应前后气体相对分子质量都大于18,所以d1>d2.
故答案为:a≥2;大于;
(3)当SO2、S同时有时;①、②反应都发生,a取值必为
| 2 |
| 3 |
设反应过程是向a L H2S中逐渐通入O2,先发生反应②,O2未用完.所生成物量用H2S计算:即S=a mol,H2O=a mol,
耗O2=
| a |
| 2 |
| a |
| 2 |
由反应可知,生成n(SO2)=n(O2)=(1-
| a |
| 2 |
反应生成气体总量为n(SO2)+n(H2O)=1-
| a |
| 2 |
| a |
| 2 |
故答案为:
| 2 |
| 3 |
| a |
| 2 |
| a |
| 2 |
点评:本题考查范围讨论题的计算,题目难度较大,注意根据反应方程式,用数轴法分析较为直观.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
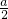 摩.(以含a的代数式表示)
摩.(以含a的代数式表示) 摩.(以含a的代数式表示)
摩.(以含a的代数式表示)