题目内容
【题目】下列有关电解质溶液的说法正确的是( )
A. 加热0. l mol·L-1的Na2CO3溶液,CO32-的水解程度和溶液的pH均增大
B. 一定温度下,CH3COOH稀溶液加水稀释后,溶液中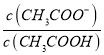 减小
减小
C. 常温下,pH=3的HF溶液与pH=11的NaOH溶液等体积混合,所得溶液的pH>7
D. 一定温度下,向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中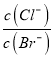 增大
增大
【答案】A
【解析】A.盐类水解是吸热反应,加热促进水解,CO32-的水解程度和溶液的pH均增大,故A正确;B.CH3COOH稀溶液加水稀释后,溶液中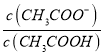 =
=![]() ,c(H+)减小,Ka不变,则溶液中
,c(H+)减小,Ka不变,则溶液中 增大,故B错误;C.pH值为3的HF和pH为11的NaOH溶液,两溶液中c(OH-)和c(H+)相等,但HF为弱酸,不能完全电离,所以HF浓度大,反应后酸过量,则混合溶液呈酸性,pH小于7,故C错误;D.AgCl、AgBr的饱和溶液中存在AgCl(s)+Br-AgBr(s)+Cl-,该反应的平衡常数K=
增大,故B错误;C.pH值为3的HF和pH为11的NaOH溶液,两溶液中c(OH-)和c(H+)相等,但HF为弱酸,不能完全电离,所以HF浓度大,反应后酸过量,则混合溶液呈酸性,pH小于7,故C错误;D.AgCl、AgBr的饱和溶液中存在AgCl(s)+Br-AgBr(s)+Cl-,该反应的平衡常数K= ,向溶液中加入少量AgNO3,K不变,故D错误,答案为A。
,向溶液中加入少量AgNO3,K不变,故D错误,答案为A。

练习册系列答案
相关题目