题目内容
在常压,150℃时,某气态烃与过量氧气的混合气体aL,点燃后并恢复至原来的条件,体积仍为aL.然后将燃烧产物通过浓硫酸,体积减少bL,再通过NaOH溶液,体积又减少bL,最后剩有少量尾气.该烃的分子式是______.
【答案】分析:该气态烃的组成为CxHy,燃烧方程式为CxHy+(x+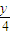 )O2
)O2 xCO2+
xCO2+ H2O,点燃后并恢复至原来的条件,水是气态,体积不变,则有1+x+
H2O,点燃后并恢复至原来的条件,水是气态,体积不变,则有1+x+ =x+
=x+ ;然后将燃烧产物通过浓硫酸,浓硫酸吸水,体积减少bL为生成的H2O的体积,再通过NaOH溶液,体积又减少bL,NaOH溶液吸收CO2,即CO2体积为bL,水的体积大于二氧化碳的体积,故烃中C、H原子数目比为1:2,据此计算确定.
;然后将燃烧产物通过浓硫酸,浓硫酸吸水,体积减少bL为生成的H2O的体积,再通过NaOH溶液,体积又减少bL,NaOH溶液吸收CO2,即CO2体积为bL,水的体积大于二氧化碳的体积,故烃中C、H原子数目比为1:2,据此计算确定.
解答:解:该气态烃的组成为CxHy,燃烧方程式为CxHy+(x+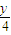 )O2
)O2 xCO2+
xCO2+ H2O,点燃后并恢复至原来的条件,水是气态,体积不变,则有1+x+
H2O,点燃后并恢复至原来的条件,水是气态,体积不变,则有1+x+ =x+
=x+ ,解得x=4,即分子中H原子数目为4;然后将燃烧产物通过浓硫酸,浓硫酸吸水,体积减少bL为生成的H2O的体积,再通过NaOH溶液,体积又减少bL,NaOH溶液吸收CO2,即CO2体积为bL,水的体积大于二氧化碳的体积,故烃中C、H原子数目比为1:2,所以分子中C原子数目为
,解得x=4,即分子中H原子数目为4;然后将燃烧产物通过浓硫酸,浓硫酸吸水,体积减少bL为生成的H2O的体积,再通过NaOH溶液,体积又减少bL,NaOH溶液吸收CO2,即CO2体积为bL,水的体积大于二氧化碳的体积,故烃中C、H原子数目比为1:2,所以分子中C原子数目为 ×4=2,故该烃的分子式为C2H4.
×4=2,故该烃的分子式为C2H4.
故答案为:C2H4.
点评:考查烃的燃烧规律、有机物分子式的确定等,难度不大,注意燃烧通式的利用.
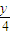 )O2
)O2 xCO2+
xCO2+ H2O,点燃后并恢复至原来的条件,水是气态,体积不变,则有1+x+
H2O,点燃后并恢复至原来的条件,水是气态,体积不变,则有1+x+ =x+
=x+ ;然后将燃烧产物通过浓硫酸,浓硫酸吸水,体积减少bL为生成的H2O的体积,再通过NaOH溶液,体积又减少bL,NaOH溶液吸收CO2,即CO2体积为bL,水的体积大于二氧化碳的体积,故烃中C、H原子数目比为1:2,据此计算确定.
;然后将燃烧产物通过浓硫酸,浓硫酸吸水,体积减少bL为生成的H2O的体积,再通过NaOH溶液,体积又减少bL,NaOH溶液吸收CO2,即CO2体积为bL,水的体积大于二氧化碳的体积,故烃中C、H原子数目比为1:2,据此计算确定.解答:解:该气态烃的组成为CxHy,燃烧方程式为CxHy+(x+
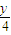 )O2
)O2 xCO2+
xCO2+ H2O,点燃后并恢复至原来的条件,水是气态,体积不变,则有1+x+
H2O,点燃后并恢复至原来的条件,水是气态,体积不变,则有1+x+ =x+
=x+ ,解得x=4,即分子中H原子数目为4;然后将燃烧产物通过浓硫酸,浓硫酸吸水,体积减少bL为生成的H2O的体积,再通过NaOH溶液,体积又减少bL,NaOH溶液吸收CO2,即CO2体积为bL,水的体积大于二氧化碳的体积,故烃中C、H原子数目比为1:2,所以分子中C原子数目为
,解得x=4,即分子中H原子数目为4;然后将燃烧产物通过浓硫酸,浓硫酸吸水,体积减少bL为生成的H2O的体积,再通过NaOH溶液,体积又减少bL,NaOH溶液吸收CO2,即CO2体积为bL,水的体积大于二氧化碳的体积,故烃中C、H原子数目比为1:2,所以分子中C原子数目为 ×4=2,故该烃的分子式为C2H4.
×4=2,故该烃的分子式为C2H4.故答案为:C2H4.
点评:考查烃的燃烧规律、有机物分子式的确定等,难度不大,注意燃烧通式的利用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目