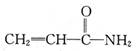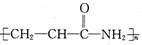题目内容
下列各组分子中,均含有非极性键且属于非极性分子的是
| A.C2H2、NH3 | B.Cl2、C2H4 | C.CO2、H2S | D.CH4、H2O2 |
B
试题分析:同种元素之间形成非极性共价键,不同元素之间形成极性共价键,分子中正负电荷中心不重合,从整个分子来看,电荷的分布是不均匀的,不对称的,这样的分子为极性分子,以极性键结合的双原子一定为极性分子,以极性键结合的多原子分子如结构对称,正负电荷的重心重合,电荷分布均匀,则为非极性分子。A、C2H2中含有极性键和非极性键,是直线型分子,结构对称,分子中正负电荷重心重叠,为非极性分子;NH3中含有极性键,空间结构为三角锥形,正负电荷的中心不重合,属于极性分子,故A错误;B、Cl2为直线形结构,含有非极性键,正负电荷的重心重合,电荷分布均匀,为非极性分子;C2H4中含有极性键和非极性键,是平面型分子,结构对称,分子中正负电荷重心重叠,为非极性分子,故B正确;C、CO2中含有极性键,为直线形分子,结构对称,分子中正负电荷重心重叠,为非极性分子;H2S中含有极性键,空间结构为v形,正负电荷的中心不重合,属于极性分子,故C错误;D、H2O2中含有极性键和非极性键,但结构不对称,正负电荷的中心不重合,属于极性分子;CH4分子中含有极性键,空间结构为正四面体形,正负电荷的中心重合,属于非极性分子,故D错误;故选B。

练习册系列答案
相关题目



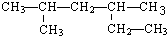 名称是______
名称是______ 中标有“·”的碳原子的杂化方式依次为
中标有“·”的碳原子的杂化方式依次为