题目内容
【题目】关于化学键的叙述中,正确的是( )
A.HCl电离产生H+和Cl﹣ , 可判断HCl分子中存在离子键
B.Na2O2固体中含有的阴离子与阳离子的个数比为1:1
C.化学键是指使原子或离子相互结合的作用力
D.不同元素组成的多原子分子中的化学键一定全是极性键
【答案】C
【解析】解:A.HCl中只存在共价键,属于共价化合物,在水分子的作用下电离出阴阳离子,故A错误;B.过氧化钠中阴阳离子个数比为1:2,故B错误;
C.化学键是指使原子或离子相互结合的作用力,相互作用力包含吸引力和排斥力,故C正确;
D不同元素组成的多原子分子中可能存在非极性键,如:乙烯中含有非极性键,故D错误;
故选C.

【题目】氮氧化物排放是形成臭氧层空洞、酸雨、雾霾的重要成因之一
I.NO和CO气体均为汽车尾气的成分,目前降低尾气的可行方法是在汽车排气管上安装催化转化器,这两种气体在催化转换器中发生反应:2CO(g)+2NO(g)![]() N2(g)+2CO2(g) △H
N2(g)+2CO2(g) △H
已知反应中相关键能数据如下:
化学键 | C | N | N | C=O |
键能/kJ·mol-1 | 1076 | 632 | 946 | 750 |
(1)由此计算△H=__________。
(2)在一定温度下,将2.0molNO、2.4molCO通入到容积固定为2L的密闭容器中,反应过程中部分物质的浓度变化如图所示:
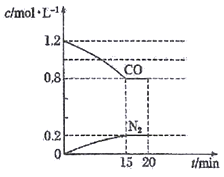
①有害气体NO的转化率为__________。
②20min时,若改变反应条件,导致CO浓度减小,则改变的条件可能是__________ (填序号)。
a.缩小容器体积 b.催化剂 c.降低温度 d.再通入2.0molNO
③若保持反应体系的温度不变,20min时再向容器中充入NO、N2各0.4mol,平衡将__________ (填“正向”或“逆向”)移动。
Ⅱ.SCR(选择性催化还原)脱硝法是工业上消除氮氧化物的常用方法,反应原理为:4NO(g)+4NH3(g)+O2(g)![]() 4N2(g)+6H2O(g)△H<0
4N2(g)+6H2O(g)△H<0
(3)该法可能发生副反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),减少副反应的主要措施是___________(写一条即可)。
4NO(g)+6H2O(g),减少副反应的主要措施是___________(写一条即可)。
(4)其他条件相同,在甲、乙两种催化剂作用下,NO转化率与温度的关系如图。
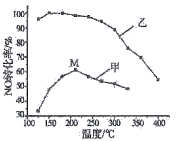
①工业上选择催化剂__________(填“甲”或“乙”),原因是____________。
②在催化剂甲作用下,图中M点处(对应温度为210℃)NO的转化率______(填“可能是”、“一定是”或“一定不是”)该温度下的平衡转化率。高于210℃时,NO转化率降低的原因可能是__________。(写一条即可)
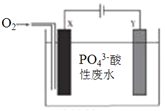
【题目】工业上以砷烟灰(主要含PbO、As2S3、In2O2、In2S3等) 为原料回收稀散金属铟(In)。铟是稀缺资源,主要应用于在透明导电涂层、荧光材料、有机合成等,铟的逆流氧化酸浸工艺流程及工艺条件如下:
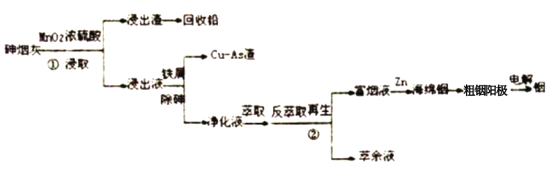
砷烟灰的逆流氧化酸浸工艺条件
项目 | 液固比 | 始酸酸度(g·L-l) | 终酸酸度(g·L-l) | 温度(℃) | 时间(h) | 锰粉加入量(%) |
一次浸出 | 3~7:1 | 90-120 | 30-80 | >95 | >4 | 3~7 |
二次浸出 | 3~7:1 | 150-180 | 120-150 | >95 | >4 | 10-15 |
(1) 流程中要多次进行混合物的分离,其中操作①的分离方法分别为_________,②的分离方法在实验室中使用的主要仪器为_________ 。
(2)下列有关流程说法不正确的是_________。
A.两次浸取时温度越高,浸出时间越长,工业效益越好
B.浸取时采用适宜的液固比,既可为下步萃取提供合适的酸度,又能得到较高浓度的In3+溶液
C.净化液通过萃取、反萃取、再生等过程可富集得到高浓度In3+溶液并使萃取剂循环利用
D.电解粗铟时阳极泥成分包括锌、铜、银等金属
(3)萃取净化液所用苯取剂可用H2A2表示,使In3+进入有机相,相关反应可表示为: In3++3H2A2![]() In (HA2)3+3H+, 则反萃取所用试剂应选用_______(选 填:“ 稀硫酸”或“NaOH溶液”)
In (HA2)3+3H+, 则反萃取所用试剂应选用_______(选 填:“ 稀硫酸”或“NaOH溶液”)
(4)砷烟灰中的As2S3不溶于稀硫酸,但加入MnO2后可溶解,并转化为AsO43-,同时产生臭鸡蛋气味气体。该反应的化学方程式为______________。
(5)电解精炼粗铟时阴极材料应选用________,随着电解的不断进行,电解液中c(In3+)会逐渐________(填:“增大”、“减小”或“不变”)。
(6)工业上常采用ITO靶材废料回收铟,其浸出液中主要含Sn4+杂质,除杂可采用加入Na2S溶液的方法。要使Sn4+沉淀完全即c(Sn4+)低于10-5mol/L,