题目内容
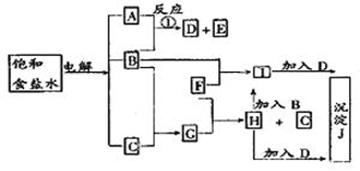
下图中的每一方格表示有关的一种反应物或生成物,其中粗框表示初始反应物(反应时加入或生成的水,以及生成沉淀J时的其他产物均已略去)。
请填写图中空白:
(1)物质B是___________,F是___________,J是___________。
(2)反应①的离子方程式是_________________。
解析:食盐水电解时生成3种产物:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑。3种产物中B既能与A反应,又能与C反应,刚可确定B为Cl2。Cl2与NaOH和H2分别发生如下反应:Cl2+2NaOH====NaCl+NaClO+H2O,Cl2+H2====2HCl。因Cl2与A有两种产物(水略去),故A为NaOH,C为H2,而G为HCl(溶于水为盐酸)。
2NaOH+H2↑+Cl2↑。3种产物中B既能与A反应,又能与C反应,刚可确定B为Cl2。Cl2与NaOH和H2分别发生如下反应:Cl2+2NaOH====NaCl+NaClO+H2O,Cl2+H2====2HCl。因Cl2与A有两种产物(水略去),故A为NaOH,C为H2,而G为HCl(溶于水为盐酸)。
从图中可以看出,F与Cl2可反应,又与HCl(盐酸)反应产生H2,且H与Cl2反应后变I,可以认定F应为Fe,H为FeCl2,I为FeCl3,同时也可确定D应为NaClO(因NaCl与FeCl3、FeCl2不反应),E为NaCl。对J的判定,要明白NaClO的两种重要性质,其一,它含有的ClO-具有强氧化性,能将Fe2+氧化;其二,HClO是比碳酸还弱的酸,NaClO可与FeCl3发生双水解。这样J也就很容易确定为Fe(OH)3。
答案:(1)Cl2 Fe Fe(OH)3 (2)Cl2+2OH-====Cl-+ClO-+H2O

下图中的每一方格表示有关的一种反应物或生成物,其中甲、乙、丙、丁为常见单质,其余均为化合物,A是一种常见的液态化合物,B是具有磁性的氧化物,D和丁既能和酸反应又能和碱反应,乙在丙中燃烧产生苍白色火焰,它们的转化关系如下:(有些反应的条件和部分产物未注明)
 |
(1)上述反应中属于氧化还原反应的是 (填写序号)
(2)写出下列物质化学式:B ,D ,F ;
(3)写出反应的化学方程式:A+甲
(4)H在空气中很容易被氧化成I,该过程的实验现象是 ; 将足量的CO2通入E溶液中,离子方程式是 。