题目内容
下列图示与对应叙述相符合的是
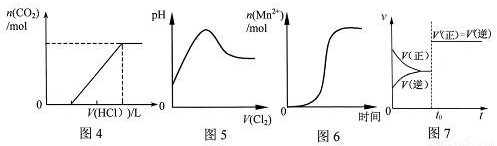
A.图1表示在含等物质的量NaOH、Na2CO3的混合溶液中滴加0.1mol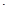
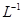 盐酸至过量时,产生气体的体积与消耗盐酸的关系
盐酸至过量时,产生气体的体积与消耗盐酸的关系
B.图2表示C12通入H2S溶液中pH的变化
C.图3表示10mL0.01mol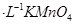 酸性溶液氧化0.1mol
酸性溶液氧化0.1mol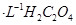 溶液时,
溶液时, 随时间的变化(M
随时间的变化(M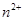 对该反应有催化作用)
对该反应有催化作用)
D.图4表示已达平衡某反应,在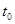 时改变某一条件后反应速率随时间变化,则改变的条件一定是加入催化剂
时改变某一条件后反应速率随时间变化,则改变的条件一定是加入催化剂
【答案】
C
【解析】
试题分析: A、滴加盐酸先后发生反应:NaOH+HCl=NaCl+H2O、Na2CO3+HCl=NaCl+NaHCO3、NaHCO3+HCl=NaCl+CO2+H2O,根据化学方程式可以开出不产生气体阶段所需盐酸体积与生成气体阶段所需盐酸体积之比为:2:1,错误;B、Cl2与H2S发生反应:Cl2+H2S=2HCl+S,由弱酸生成强酸,pH降低,错误;C、生成Mn2+,具有催化作用,化学反应速率加快,正确;D、对于反应前后气体系数相等的反应,反应速率的变化也符合图4,错误。
考点: 本题重要物质的性质和化学反应速率。

练习册系列答案
相关题目
下列图示与对应叙述相符合的是( )


| A、图1表示在含等物质的量NaOH、Na2CO3的混合溶液中滴加0.1mol?L-1盐酸至过量时,产生气体的体积与消耗盐酸的关系 | B、图2表示Cl2通入SO2溶液中pH的变化 | C、图3表示10 mL 0.01 mol?L-1KMnO4 酸性溶液与过量的0.1 mol?L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化(Mn2+对该反应有催化作用) | D、图4表示已达平衡的某可逆反应,在t0时改变某一条件后反应速率随时间变化,则改变的条件一定是加入催化剂 |

 ( )
( )