题目内容
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中A的原子最外层电子数是次外层电子数的2倍,元素B的原子最外层电子数是其电子层数的3倍,D与A为同主族元素,元素C与E形成的化合物CE是厨房常用调味品。下列说法正确的是
A.原子半径:C>D>B>A
B.A、D、E最高价氧化物对应水化物酸性增强
C.只含B元素的物质一定是纯净物
D.化合物C2AB3的水溶液显碱性,可用于洗去铜片表面的油污
D
解析试题分析:根据题意可知:A是C;B是O;C是Na;D是Si;E是Cl.A.C、O都是第二周期的元素;Na、Si都是第三周期的元素。同一周期的元素,原子序数越大,原子半径就越小;不同周期的元素,元素原子的核外电子层数越多,原子半径就越大。因此原子半径为Na>Si>C> O。错误。B.元素的非金属性越强,其最高价氧化物对应的水化物的酸性就越强,元素的非金属性:Cl >C>Si,所以酸性HClO4>H2CO3>H2SiO3。错误。C.只含B元素的物质可能是O2、O3或它们的混合物,因此不一定是纯净物。错误。D.化合物Na2CO3是强碱弱酸盐。弱酸根离子水解使的水溶液显碱性,由于碱能够跟油脂发生反应变为容易溶解于水的物质,所以可用于洗去铜片表面的油污。正确。
考点:考查元素的推断、元素及形成的化合物的性质的知识。

 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案2008年秋天,毒奶粉事件震惊全国,这主要是奶粉中含有有毒的三聚氰胺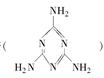 。下列关于三聚氰胺分子的说法正确的是
。下列关于三聚氰胺分子的说法正确的是
| A.所有碳原子采用sp3杂化,所有氮原子采用sp3杂化 |
| B.一个分子中共含有15个σ键 |
| C.属于极性分子,故极易溶于水 |
| D.分子内既有极性键又有非极性键 |
下列各微粒中,各个电子层电子数都达到2n2个的是
| A.Ne、Ar | B.Al3+、S2- | C.F-、Na+ | D.He、Cl- |
下列比较错误的是
| A.原子半径:N>O>F |
| B.酸性强弱:HNO3>H3PO4>H2SO4 |
| C.碱性强弱:KOH >NaOH>Mg(OH)2 |
| D.氢化物的稳定性:HF>HCl>H2S |
下图是元素周期表的一部分,下列说法正确的是( )
| A.可在灰色区域“甲”中寻找催化剂 |
| B.离子半径:W-﹥Y3-﹥X+ |
| C.气态氢化物的稳定性:Z﹥W |
| D.工业上电解X和W化合物的水溶液制备X |
甲乙两种非金属,能说明甲的非金属性一定比乙强的是
| A.甲与金属反应时得电子的数目比乙多 |
| B.甲单质的熔沸点比乙的低 |
| C.甲的氧化物对应的水化物酸性比乙强 |
| D.甲能将乙的简单离子从其盐溶液中置换出来 |
第三周期元素,浓度均为0.01 mol/L的最高价氧化物对应水化物的pH与原子半径的关系如图所示。则下列说法正确的是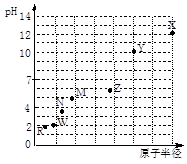
| A.气态氢化物的稳定性:N>R |
| B.Z的最高价氧化物对应的水化物能溶于稀氨水 |
| C.Y和R形成的化合物既含离子键又含共价键 |
| D.X和M两者最高价氧化物对应的水化物反应后溶液的pH>7 |
短周期元素X、Y、Z关系如图,X原子的电子层数为n,最外层电子数为2n。W原子最内层电子数是最外层电子数的2倍。下列说法错误的是
| X | | | |
| | | Y | Z |
A.X 和Y都是非金属元素,其中X最高化合价为+5价
B.X、W的最高价氧化物在一定条件下能反应
C.元素X、W和氧元素可形成化学式为W2XO3共价化合物
D.Y、Z的氢化物的稳定性:Y<Z
四种短周期元素W、X、Y、Z的原子序数依次递增,X的一种单质能在空气中自燃。电解含有Y和Z的阴离子的混合溶液时,在阳极Y离子先失去电子。W和Z同主族。对于这四种元素下列判断正确的是
| A.气态氢化物的稳定性:W>X>Y>Z |
| B.单质的氧化性:W>Z>Y>X |
| C.四种元素原子半径大小:W<Y<Z<X |
| D.W单质可以将Z从其盐溶液中置换出来 |