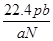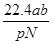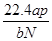题目内容
(6分)在标准状况下,将224L HCl气体溶于635mL水(ρ=1.00g·cm-3)中,所得盐酸的密度为1.18g·cm-3。此溶液物质的量浓度应该为多少?若取出这种盐酸10.0mL,向其中加水配制成1L溶液,则所得稀盐酸的物质的量浓度应该为多少?
36.5%;11.8mol·L-1;0. 118mol·L-1(6分)
考查物质的量浓度的有关计算。
氯化氢的物质的量是224L÷22.4L/mol=10mol
质量是10mol×36.5g/mol=365g
所以盐酸的质量分数是
w(HCl)=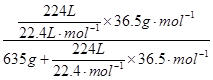 ×100%=36.5%
×100%=36.5%
又因为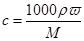
所以c(HCl)=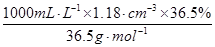 =11.8mol·L-1
=11.8mol·L-1
由于在稀释过程中溶质的物质的量是不变的
所以稀释后溶液的浓缩是
c(稀HCl)=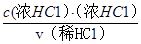 =
=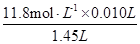 =0. 118mol·L-1
=0. 118mol·L-1
氯化氢的物质的量是224L÷22.4L/mol=10mol
质量是10mol×36.5g/mol=365g
所以盐酸的质量分数是
w(HCl)=
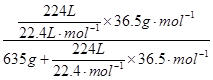 ×100%=36.5%
×100%=36.5%又因为
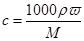
所以c(HCl)=
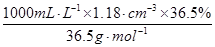 =11.8mol·L-1
=11.8mol·L-1 由于在稀释过程中溶质的物质的量是不变的
所以稀释后溶液的浓缩是
c(稀HCl)=
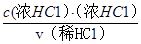 =
=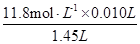 =0. 118mol·L-1
=0. 118mol·L-1
练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目