题目内容
将1molCO和1 molNO2冲入密闭容器中,在催化剂存在下发生反应:NO2(g)+CO(g) NO(g)+CO2(g)并达到化学平衡,发现有50%的CO 转化为CO2。在其他条件不变的情况下,若将1molCO 和2 molNO2 充入上述容器中,则反应达到化学平衡时,混合气体中的CO2的体积分数是
NO(g)+CO2(g)并达到化学平衡,发现有50%的CO 转化为CO2。在其他条件不变的情况下,若将1molCO 和2 molNO2 充入上述容器中,则反应达到化学平衡时,混合气体中的CO2的体积分数是
 NO(g)+CO2(g)并达到化学平衡,发现有50%的CO 转化为CO2。在其他条件不变的情况下,若将1molCO 和2 molNO2 充入上述容器中,则反应达到化学平衡时,混合气体中的CO2的体积分数是
NO(g)+CO2(g)并达到化学平衡,发现有50%的CO 转化为CO2。在其他条件不变的情况下,若将1molCO 和2 molNO2 充入上述容器中,则反应达到化学平衡时,混合气体中的CO2的体积分数是| A.1/9 | B.1/6 | C.2/9 | D.1/3 |
C
方程式:NO2(g)+CO(g) NO(g)+CO2(g)
NO(g)+CO2(g)
起始物质的量: 1mol 1mol 0 0
变化物质的量: 0.5mol 0.5mol 0.5mol 0.5mol
平衡物质的量: 0.5mol 0.5mol 0.5mol 0.5mol
即可得在该温度下K=1;所以,当将1molCO 和2 molNO2 充入上述容器中则
由化学反应方程式NO2(g)+CO(g) NO(g)+CO2(g)
NO(g)+CO2(g)
起始物质的量: 2mol 1mol 0 0
变化物质的量: x x x x
平衡物质的量: (2-x)mol (1-x)mol x x
则由K=1;得X= ,即可得混合气体中的CO2的体积分数是2/9
,即可得混合气体中的CO2的体积分数是2/9
 NO(g)+CO2(g)
NO(g)+CO2(g)起始物质的量: 1mol 1mol 0 0
变化物质的量: 0.5mol 0.5mol 0.5mol 0.5mol
平衡物质的量: 0.5mol 0.5mol 0.5mol 0.5mol
即可得在该温度下K=1;所以,当将1molCO 和2 molNO2 充入上述容器中则
由化学反应方程式NO2(g)+CO(g)
 NO(g)+CO2(g)
NO(g)+CO2(g)起始物质的量: 2mol 1mol 0 0
变化物质的量: x x x x
平衡物质的量: (2-x)mol (1-x)mol x x
则由K=1;得X=
 ,即可得混合气体中的CO2的体积分数是2/9
,即可得混合气体中的CO2的体积分数是2/9
练习册系列答案
相关题目
 cC(s)+dD,当反应进行一定时间
cC(s)+dD,当反应进行一定时间 后,测得A减少了nmol,B减少了1/2 n mol,C增加了3/2 n mol,D增加了n mol,此时达到化学平衡。请填写下列空白:
后,测得A减少了nmol,B减少了1/2 n mol,C增加了3/2 n mol,D增加了n mol,此时达到化学平衡。请填写下列空白: 反应一段时间后,测知四种物质其物质的量又达到相等,则该反应为________反应(填“放热”或“吸热”)。
反应一段时间后,测知四种物质其物质的量又达到相等,则该反应为________反应(填“放热”或“吸热”)。 C(g) +2D(g) △H<0在一定条件下达到平衡,下列有关叙述正确的是( )
C(g) +2D(g) △H<0在一定条件下达到平衡,下列有关叙述正确的是( ) H2(g)+I2(g)]时,I2的体积分数为X%;相同条件下,2 mol HI分解达平衡时,I2的体积分数为Y%,则X与Y的关系为
H2(g)+I2(g)]时,I2的体积分数为X%;相同条件下,2 mol HI分解达平衡时,I2的体积分数为Y%,则X与Y的关系为 N2O3+O2,②N2O3
N2O3+O2,②N2O3
 CH3OH(g)。
CH3OH(g)。
 2 NH3(g),平衡时混合气体共7 mol.令a、b、c分别代表N2、H2、NH3起始加入的物质的量,维持温度不变,使达到平衡时各成分的百分含量不变.则:
2 NH3(g),平衡时混合气体共7 mol.令a、b、c分别代表N2、H2、NH3起始加入的物质的量,维持温度不变,使达到平衡时各成分的百分含量不变.则: Z(g)+2W(g) △H<0。达到平衡(Ⅰ)时,B中密度变为原来的
Z(g)+2W(g) △H<0。达到平衡(Ⅰ)时,B中密度变为原来的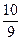 ,试回答:
,试回答:
 ,H2(g)+CO2(g)
,H2(g)+CO2(g) H2O(g)+CO(g)的平衡常数K=
H2O(g)+CO(g)的平衡常数K= 。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示:
。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示: 0
0