题目内容
5.芳香族化合物G与 互为同分异构体,G的苯环上的一氯代物只有一种结构,则G可能的结构有( )
互为同分异构体,G的苯环上的一氯代物只有一种结构,则G可能的结构有( )| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |
分析 G苯环上的一氯代物只有一种结构,则环上的取代基具有高度的对称性,即 ,其中四个取代基连接甲基与溴原子,两个取代基的连接-CH2Br,据此确定结构.
,其中四个取代基连接甲基与溴原子,两个取代基的连接-CH2Br,据此确定结构.
解答 解:G苯环上的一氯代物只有一种结构,则环上的取代基具有高度的对称性,即 ,其中四个取代基连接2个甲基与2个溴原子,每种结构都有2种情况,共6种结构,两个取代基的连接2个-CH2Br,只有1种结构,所以共7种结构,故选C.
,其中四个取代基连接2个甲基与2个溴原子,每种结构都有2种情况,共6种结构,两个取代基的连接2个-CH2Br,只有1种结构,所以共7种结构,故选C.
点评 本题主要考查同分异构体的书写,根据等效氢判断侧链是解题的关键,题目难度中等.

练习册系列答案
相关题目
15.乙烯雌酚是一种激素类药物,结构简式如图:下列说法正确的是( )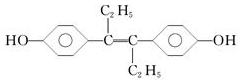

| A. | 分子式为C18H20O2,具有弱酸性 | |
| B. | 分子中只含有羟基一种官能闭 | |
| C. | 该分子不存在顺反异构 | |
| D. | 与浓溴水只发生加成反应,不能发生取代反应 |
16.下列各物质中,一定不能使溴水和高锰酸钾酸性溶液褪色的是( )
| A. | C5H10 | B. | C4H8 | C. | C3H6 | D. | C2H6 |
13.已知N2+3H2?2NH3为放热反应,对该反应的下列说法中正确的是( )
| A. | N2的能量一定高于NH3 | |
| B. | H2的能量一定高于NH3 | |
| C. | 1 mol N2和3 mol H2的总能量一定高于2 mol NH3的总能量 | |
| D. | 因该反应为放热反应,故不必加热就可发生 |
10.下列化合物的同类同分异构体数目为5种的是(不考虑立体异构)( )
| A. | 己烷C6H14 | B. | 戊醛C5H10O | C. | 丙醇C3H8O | D. | 一氯戊烷C5H12Cl |
17.从镍矿石尾矿中提取NiSO4是解决我国镍资源匮乏的一条重要途径,已知该过程如图:

表1:各物质的Ksp数据如表:
表2:滤液A中各金属离子的含量如表:
根据以上信息,回答下列问题:
(1)步骤Ⅰ酸浸之前需将矿石粉碎,目的是增大接触面积,提高浸取率
(2)若杂质离子的浓度c≤1.0×10-5mol/L即可认定沉淀完全,则步骤中当Pb2+恰好沉淀完全时,溶液中硫离子的浓度c(S2-)=8.0×10-23;此时Ni2+是否已开始沉淀否(填“是”或“否”).
(3)常温下进行步骤Ⅲ的目的是为了除去铁和锰元素,已知除铁元素的离子反应如下:
2Fe2++ClO-+5H2O=2Fe(OH)3↓+Cl-+4H+
此时Mn2+的氧化产物为MnO2,写出除锰元素的离子方程式Mn2++ClO-+H2O=MnO2+Cl-+2H+.
(4)为测定滤液A中Fe2+离子的含量,每次移取20.00mL待测液,并用0.02mol/L的KMnO4溶液滴定,若已知其他离子均不反应,且三次滴定平均消耗KMnO4溶液18.00mL,则x的值为5.04g/L(精确到小数点后两位).
(5)所得Ni(OH)2是制造镍铬电池的重要原料,镍镉电池工作原理如下:
Cd+2NiO(OH)+2H2O$?_{充电}^{放电}$2Cd(OH)2+2Ni(OH)2
则随着放电的进行,正极区pH增大(填“增大”、“减小”或“不变”);充电时阴极电极反应式为Cd(OH)2+2e-=Cd+2OH-.

表1:各物质的Ksp数据如表:
| 物质 | MnS | NiS | PbS | CuS | Ni(OH)2 |
| Ksp | 2.5×10-13 | 1.1×10-21 | 8.0×10-28 | 6.3×10-36 | 2.0×10-15 |
| 成分 | Ni2+ | Fe3+ | Fe2+ | Mn2+ | Cu2+ | Pb2+ | … |
| 含量(g/L) | 3.80 | 4.80 | x | 0.20 | 0.15 | <0.001 | … |
(1)步骤Ⅰ酸浸之前需将矿石粉碎,目的是增大接触面积,提高浸取率
(2)若杂质离子的浓度c≤1.0×10-5mol/L即可认定沉淀完全,则步骤中当Pb2+恰好沉淀完全时,溶液中硫离子的浓度c(S2-)=8.0×10-23;此时Ni2+是否已开始沉淀否(填“是”或“否”).
(3)常温下进行步骤Ⅲ的目的是为了除去铁和锰元素,已知除铁元素的离子反应如下:
2Fe2++ClO-+5H2O=2Fe(OH)3↓+Cl-+4H+
此时Mn2+的氧化产物为MnO2,写出除锰元素的离子方程式Mn2++ClO-+H2O=MnO2+Cl-+2H+.
(4)为测定滤液A中Fe2+离子的含量,每次移取20.00mL待测液,并用0.02mol/L的KMnO4溶液滴定,若已知其他离子均不反应,且三次滴定平均消耗KMnO4溶液18.00mL,则x的值为5.04g/L(精确到小数点后两位).
(5)所得Ni(OH)2是制造镍铬电池的重要原料,镍镉电池工作原理如下:
Cd+2NiO(OH)+2H2O$?_{充电}^{放电}$2Cd(OH)2+2Ni(OH)2
则随着放电的进行,正极区pH增大(填“增大”、“减小”或“不变”);充电时阴极电极反应式为Cd(OH)2+2e-=Cd+2OH-.
14.下列变化中,不属于化学变化的是( )
| A. | 煤的气化 | B. | 石油分馏 | C. | 石油裂解 | D. | 煤的干馏 |
15.载人空间站的生态系统中.要求分离人呼出的二氧化碳,同时需要提供氧气.某电化学装置利用太阳能转化的电能可以实现上述要求,同时还有燃料一氧化碳生成,该电化学装置的总反应为2CO2$\frac{\underline{\;电解\;}}{\;}$2CO+O2.下列判断错误的是( )
| A. | 该装置的阴极反应式是2CO2+4e-+2H2O=2CO+4OH- | |
| B. | 该装置的阳极反应式是4OH--4e-=2H2O+O2↑ | |
| C. | 每处理44 g CO2,可得到22.4 LCO 和11.2L O2 | |
| D. | 反应结束后电解池溶液的pH保待不变 |