题目内容
(1)现有500mL物质的量浓度为1mol/L的NaOH溶液,与足量的铝完全反应,可消耗多少克铝?
(2)若产生标准状况下11.2L的H2,转移多少mol电子?
(2)若产生标准状况下11.2L的H2,转移多少mol电子?
(1)13.5 (2)1mol
试题分析:2Al+2NaOH+2H2O=2NaAlO2+3H2

2 2
X 0.5L×1mol/L 解得:X=0.5mol
m(Al)=0.5mol×27g/mol=13.5g
(2)若产生标准状况下11.2L的H2,则0.5mol,转移的电子即为1mol。
点评:化学计量是学习化学的基础,考生应熟练掌握公式,灵活应用。注意解题格式及单位。

练习册系列答案
相关题目
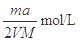
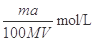
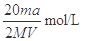
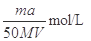
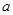 g某气体中含有的分子数为
g某气体中含有的分子数为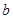 ,则
,则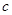 g该气体在标准状况下占有的体积应表示为(式中
g该气体在标准状况下占有的体积应表示为(式中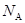 为阿伏加德罗常数)
为阿伏加德罗常数)