题目内容
下列叙述正确的是( )
| A、L层电子为偶数的所有主族元素所在族的序数与该元素原子的L层电子数相等 |
| B、最外层电子数为8的粒子是稀有气体元素的原子 |
| C、在周期表里,主族元素所在的族序数等于原子核外电子数 |
| D、周期表中L层电子为奇数的元素所在族序数与该元素原子的L层电子数相等 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:A.周期数等于或大于第三周期的主族元素,L层电子数都是8,主族族序数不等该元素原子的L层电子数;
B.最外层电子数为8的粒子可能是离子,也可能为中性原子;
C.在周期表里,主族元素所在的族序数等于其最外层电子数;
D.L层电子为奇数的所有元素为锂、硼、氮、氟.
B.最外层电子数为8的粒子可能是离子,也可能为中性原子;
C.在周期表里,主族元素所在的族序数等于其最外层电子数;
D.L层电子为奇数的所有元素为锂、硼、氮、氟.
解答:
解:A.第二周期中L层电子为偶数的所有主族元素有铍、碳、氧,主族族序数等于L层电子数,但周期数等于或大于第三周期的主族元素,L层电子数都是8,主族族序数不等该元素原子的L层电子数,故A错误;
B.最外层电子数为8的粒子可能是离子,也可能为中性原子,若为中性原子则为稀有气体原子,若为离子,则不是稀有气体原子,故B错误;
C.在周期表里,主族元素所在的族序数等于其最外层电子数,故C错误;
D.L层电子为奇数的所有元素为锂、硼、氮、氟,元素所在族的序数与该元素原子的L层电子数相等,故D正确,
故选D.
B.最外层电子数为8的粒子可能是离子,也可能为中性原子,若为中性原子则为稀有气体原子,若为离子,则不是稀有气体原子,故B错误;
C.在周期表里,主族元素所在的族序数等于其最外层电子数,故C错误;
D.L层电子为奇数的所有元素为锂、硼、氮、氟,元素所在族的序数与该元素原子的L层电子数相等,故D正确,
故选D.
点评:本题考查学生元素周期表与元素周期律,难度不大,注意利用列举法进行计算.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
用NA表示阿伏加德罗常数,下列说法正确的是( )
| A、22.4L C2H2中有2NA个π键 |
| B、1mol苯含有碳碳双键的数目为3NA |
| C、常温常压下,7.0g乙烯与丙烯的混合物中含有氢原子的数目为NA |
| D、1mol二氧化硅晶体中含Si-O键的数目为2NA |
某有机物的结构简式如图所示,下列说法中不正确的是( )
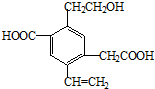

| A、1mol该有机物和过量的金属钠反应最多可以生成1.5mol H2 |
| B、该物质消耗Na、NaOH、NaHCO3的物质的量之比为3:2:2 |
| C、可以用酸性高锰酸钾溶液检验其中的碳碳双键 |
| D、该物质能够在催化剂作用下被氧化为醛 |
下列关于可逆反应达到平衡状态的描述,正确的是( )
| A、反应停止 |
| B、正、逆反应速率都为零 |
| C、各物质浓度不再改变 |
| D、反应物的浓度为零 |
下列对硫酸的叙述错误的是( )
| A、硫酸是强酸 |
| B、浓硫酸具有氧化性 |
| C、浓硫酸可作干燥剂 |
| D、稀释浓硫酸时,边搅拌浓硫酸边慢慢地加水 |
下列叙述正确的是( )
A、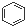 和 和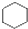 均是芳香烃, 均是芳香烃,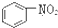 既是芳香烃又是芳香化合物 既是芳香烃又是芳香化合物 |
B、 和 和 分子组成相差一个-CH2-,因此是同系物关系 分子组成相差一个-CH2-,因此是同系物关系 |
| C、天然气、沼气、坑气、煤气的主要成分都是甲烷 |
| D、分子式为C4H10O的物质,可能属于醇类或醚类 |
在碱性溶液中能大量共存且溶液为无色透明的离子组是( )
| A、K+、MnO4-、Na+、Cl- |
| B、K+、Ba2+、NO3-、Cl- |
| C、Na+、HCO3-、NO3-、SO42- |
| D、Fe3+、Na+、Cl-、SO42- |
下列文字表述与反应方程式对应且正确的是( )
A、乙醇与乙酸在浓硫酸存在时加热的反应: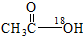 +CH3CH2OH +CH3CH2OH
 +H2O +H2O | |||
| B、碱性甲烷燃料电池的负极反应式为:CH4+10OH--8e-=CO32-+7H2O | |||
C、蔗糖在稀硫酸作催化剂时的水解反应:C12H22O11(蔗糖)+H2O
| |||
D、苯的硝化反应: +HNO3(浓) +HNO3(浓)
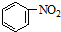 |