题目内容
常温下,下列各组离子一定能大量共存的是
| A.c(Fe3+) =0.1mol·L-1的溶液中:K+、NH4+、SCN-、SO42- |
| B.水电离出的(OH-)=1。0×10-3 mol·L-1的溶液:Na+ 、K+、MnO4-、C2O42- |
| C.能与铝反应生成氢气的溶液中:K+、Cl- 、Na+、SiO32- |
| D.0 1 mol·L-1NaOH溶液K+、Na+、SiO32-、CO32- |
D
解析试题分析:A、铁离子与SCN-不能大量共存,错误;B、MnO4-与C2O42- 发生氧化还原反应不能大量共存,错误;C、能与铝反应生成氢气的溶液中可以是酸性也可以是碱性溶液,但在酸性溶液中硅酸根离子不能大量共存,错误;D、离子之间不发生反应可以大量共存,正确,答案选D。
考点:考查离子的大量共存问题

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
铜器久置于空气中会和空气中的水蒸气、CO2、O2作用产生“绿锈”,该“绿锈”俗称“铜绿”,化学式为Cu2(OH)2CO3,“铜绿”能跟酸反应生成铜盐和CO2、H2O。某同学利用下述系列反应实现了“铜→铜绿……→铜”的转化。
(1)从三种不同分类标准回答,“铜绿”属于哪类物质?
________、________、________。
(2)请写出铜绿与盐酸反应的化学方程式_________________________________。
(3)写出B的化学式________。
(4)上述转化过程中属于化合反应的是________,属于复分解反应的是________。
(5)胶体铜在电子行业、塑料和陶瓷电镀等方面应用广泛。下列关于溶液和胶体的叙述,正确的是________。
| A.一束光线分别通过溶液和胶体时,后者能看到一条光亮的“通路”,前者则没有 |
| B.溶液是电中性的,胶体是带电的 |
| C.溶液中溶质分子可以通过滤纸,胶体中分散质粒子则不能通过滤纸 |
| D.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动 |
下列各组离子,在强酸性溶液中可以大量共存的是
| A.Na+、Ba2+、Cl-、SO32- | B.Na+、Ba2+、AlO2-、NO3- |
| C.NH4+、K+、Cl-、NO3- | D.Na+、K+、NO3-、SiO32- |
下列物质中,属于电解质的是
| A.酒精 | B.铜 | C.二氧化硫 | D.氯化钠 |
下列离子方程式中,正确的是
| A.Na2S2O3溶液中加入稀硫酸:2S2O32 -+4H+=SO42 -+3S↓+2H2O |
| B.醋酸除去水垢:2H++CaCO3=Ca2++ CO2↑+ H2O |
| C.FeS溶于过量稀硝酸中:FeS + 2H+=Fe2+ + H2↑ |
| D.双氧水中加入稀硫酸和KI溶液: H2O2+ 2I-+2H+=I2+ 2H2O |
下列离子方程式表达正确的是( )
| A.氢氧化铁溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
B.小苏打溶液呈碱性的原因:HCO3-+H2O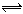 H3O++CO32- H3O++CO32- |
| C.溴化亚铁溶液中通入足量氯气:2Fe2++ 4Br-+ 3Cl2 = 2Fe3++2 Br2 + 6Cl- |
| D.向硫酸铝铵[NH4Al(SO4)2]溶液中滴加少量Ba(OH)2溶液: |
下列反应的离子方程式书写正确的是
| A.向Ba(OH)2溶液中滴入稀硫酸:H+ + OHˉ= H2O |
| B.向AlCl3溶液中滴入氨水:Al3++3OHˉ= Al(OH)3↓ |
C.向NaHCO3溶液中滴入稀盐酸:H++HCO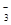 = CO2↑+H2O = CO2↑+H2O |
| D.向Fe2(SO4)3溶液中加入铁粉:Fe3++Fe = 2Fe2+ |