题目内容
6.足量镁粉与一定量的盐酸反应,由于反应太快,不易操作.为减慢反应速率,但不影响氢气的总量,可以加入下列物质中的( )| A. | 硫酸溶液 | B. | 氢氧化钠溶液 | C. | 醋酸钠固体 | D. | 碳酸钾固体 |
分析 根据发生的反应为Mg+2H+═Mg2++H2↑,则减小氢离子的浓度而不改变氢离子的物质的量即可满足减慢反应速率,但又不影响产生氢气的总量,以此来解答.
解答 解:A.加入硫酸,生成氢气的总量增大,故A错误;
B.加入NaOH,发生酸碱中和反应,减少氢气的生成,故B错误;
C.加入CH3COONa,与盐酸反应生成醋酸,氢离子浓度减小而不改变氢原子子的总物质的量即可满足减慢反应速率,但又不影响产生氢气的总量,故C正确;
D.加入K2CO3固体,与盐酸反应生成二氧化碳,减少氢气的生成,故D错误.
故选C.
点评 本题以化学反应来考查影响反应速率的因素,为高频考点,明确氢离子浓度减小是减慢反应速率的关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.下列各组物质互为同素异形体的是( )
| A. | 12C和14C | B. | H2O和D2O | C. | O2和O3 | D. | 淀粉和纤维素 |
1.如表是不同温度下水的离子积数据:
试回答以下几个问题:
(1)若25<t1<t2,则a>1×10-14(填“<”、“>”或“=”);
(2)在25℃下,0.05mol/L的Ba(OH)2溶液的pH=13;
(3)在25℃下,pH=10的NaOH溶液中,水电离产生的c(OH-)为:1×10-10mol/L;
(4)在t2℃下,将pH=9的氢氧化钠溶液V1L与pH=4的硫酸溶液V2L混合(设混合后溶液体积为原两溶液体积之和)所得溶液的pH=7,则V1:V2=$\frac{1}{9}$.
| 温度/℃ | 25 | t1 | t2 |
| Kw/mol2•L-2 | 1×10-14 | a | 1×10-12 |
(1)若25<t1<t2,则a>1×10-14(填“<”、“>”或“=”);
(2)在25℃下,0.05mol/L的Ba(OH)2溶液的pH=13;
(3)在25℃下,pH=10的NaOH溶液中,水电离产生的c(OH-)为:1×10-10mol/L;
(4)在t2℃下,将pH=9的氢氧化钠溶液V1L与pH=4的硫酸溶液V2L混合(设混合后溶液体积为原两溶液体积之和)所得溶液的pH=7,则V1:V2=$\frac{1}{9}$.
18.下列关于氧化性、还原性的判断正确的是( )
| A. | B的阳离子的氧化性比A的阳离子强,说明A元素的金属性一定比B元素强 | |
| B. | 发生氧化还原反应时,A原子失去的电子比B原子多,证明A的金属性一定比B强 | |
| C. | 适量的Cl2通入FeI2溶液中可发生反应:3Cl2+6FeI2=2FeCl3+4FeI3 | |
| D. | 一定量氯气通入30 mL 10.00 mol•L-1的氢氧化钠溶液中,加热后形成NaCl、NaClO、NaClO3共存的溶液,若反应中转移的电子为n mol,则0.15<n<0.25 |
15.下列事实与NH3极易溶于水无关的是( )
| A. | NH3与水反应生成NH3•H2O | B. | NH3与水分子之间形成氢键 | ||
| C. | NH3和水分子的相对分子质量接近 | D. | NH3是极性分子 |
16.铷和另一种碱金属的合金46g,与水完全反应,放出2g的氢气,则合金中另一种金属是( )
| A. | Li | B. | Na | C. | K | D. | Cs |
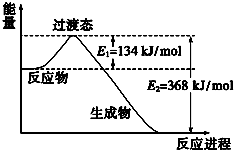 (1)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)═CO2(g)+NO(g)△H=-234kJ/mol.
(1)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)═CO2(g)+NO(g)△H=-234kJ/mol.