题目内容
【题目】有关下列实验数据判断正确的是( )
①用100mL的量筒量取16.80mL的液体
②用托盘天平称取12.50gKCl固体
③中和滴定操作时,消耗0.1000mol/L的H2SO423.0mL
④用广泛pH试纸测得某溶液的pH=3.4
A. ①④正确 B. ①③正确 C. ④正确 D. ①②③④全错
【答案】D
【解析】①量筒只能读数到0.1mL,应该用滴定管量取16.80mL的液体,错误;②托盘天平只能读数到0.1g,不能用托盘天平称取12.50gKCl固体,错误;③滴定管读数到0.01mL,错误;④用广泛pH试纸测得溶液的pH只能是整数,错误,答案选D。

 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案【题目】硼镁泥是硼镁矿生产硼砂晶体(Na2B4O7·10H2O)时的废渣,其主要成分是MgO,还含有Na2B4O7、CaO、Fe2O3 、FeO、MnO、SiO2等杂质。以硼镁泥为原料制取的七水硫酸镁在印染、造纸和医药等工业上都有广泛的应用。硼镁泥制取七水硫酸镁的工艺流程如下:
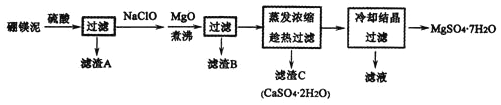
回答下列问题:
(1)Na2B4O7·10H2O中B的化合价为________________。
(2)Na2B4O7易溶于水,也较易发生水解:B4O72-+7H2O![]() 4H3BO3(硼酸)+2OH-,(硼酸在常温下溶解度较小)。写出加入硫酸时Na2B4O7发生反应的化学方程式:_________________________________。
4H3BO3(硼酸)+2OH-,(硼酸在常温下溶解度较小)。写出加入硫酸时Na2B4O7发生反应的化学方程式:_________________________________。
(3)滤渣B中含有不溶于稀盐酸但能溶于浓盐酸的黑色固体,写出生成黑色固体的离子方程式_________________。
(4)加入MgO的目的是_____________________。
(5)己知MgSO4、CaSO4的溶解度如下表:
温度(℃) 溶解度(g) | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
操作“A”是将MgSO4:和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明“操作A”步骤为____________________。
(6)Na2B4O7·10H2O失去全部结晶水后的硼砂与金属钠、氢气及石英砂一起反应可制备有机化学中的“万能还原剂——NaBH4”(该过程B的化合价不变)。
①写出NaBH4的电子式_____________。
②“有效氢含量”可用来衡量含氢还原剂的还原能力,其定义是:每克含氢还原剂的还原能力相当于多少克H2的还原能力。NaBH4的有效氢含量为_____(计算结果保留两位小数)。
③在碱性条件下,在阴极上电解NaBO2也可制得硼氢化钠,写出阴极室的电极反应式_______________。