题目内容
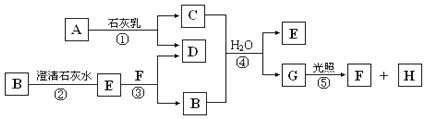
【题目】现有金属单质A和气体甲、乙、丙及物质B,C,D,E,F,G,它们之问能发生如下反应,其中乙是黄绿色气体(图中有些反应的产物和反应的条件没有全部标出). 
请根据以上信息回答下列问题:
(1)写出下列物质的名称:丙;
(2)写出下列物质的化学式:F;
(3)气体乙是一种重要的化工原料,在工农业牛产、牛活中有着重要的应用.请你根据所学知识回答下列问题:
①把气体乙通入紫色石蕊溶液中,可以观察到的现象是: , 请你解释其中的原因 .
②某化学兴趣小组计划用气体乙和物质B制取简易消毒液D.其反应原理为:(用化学方程式表示) .
【答案】
(1)氯化氢
(2)Ca(ClO)2
(3)先变红后褪色;氯气和水反应生成HCl、HClO,溶液显酸性使石蕊变红HClO具有漂白性(或强氧化性)使溶液褪色;Cl2+2NaOH=NaCl+NaClO+H2O
【解析】解:金属单质A和气体甲、乙、丙及物质B、C、D、E、F、G,乙是黄绿色气体,则乙是Cl2;A和氧气反应生成淡黄色固体G,则A是Na、G是Na2O2;A和水反应生成气体甲和B,则A是H2、B是NaOH;氢气和氯气反应生成丙为HCl,C是盐酸,浓盐酸和二氧化锰在加热条件下反应生成氯气,氯气和E反应生成F,F为漂白粉的有效成分,为Ca(ClO)2 , 所以E是Ca(OH)2 , 某化学兴趣小组计划用气体乙和物质B制取简易消毒液D,则D是NaClO和NaCl,(1)通过以上分析知,丙是氯化氢,所以答案是:氯化氢;(2)F是漂白粉的有效成分为Ca(ClO)2 , 所以答案是:Ca(ClO)2;(3)①氯气和水反应生成HCl和HClO,溶液呈酸性,HClO具有漂白性,所以将乙通入紫色石蕊试液中,酸使石蕊变红色,次氯酸使红色褪色,所以看到的现象是先变红后褪色,
所以答案是:先变红后褪色;氯气和水反应生成HCl、HClO,溶液显酸性使石蕊变红HClO具有漂白性(或强氧化性)使溶液褪色;②氯气和NaOH反应生成NaCl和NaClO,NaClO具有漂白性,发生的反应为Cl2+2NaOH=NaCl+NaClO+H2O,所以答案是:Cl2+2NaOH=NaCl+NaClO+H2O.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】生产措施与目的不相符的是
选项 | 生产措施 | 目的 |
A | 工业制硫酸:粉碎硫铁矿 | 提高反应的速率 |
B | 合成氨:铁触媒作催化剂 | 提高产物的产率 |
C | 海水提溴:热空气吹出Br2 | 提高Br2的纯度 |
D | 侯氏制碱:母液循环使用 | 提高原料利用率 |
A. AB. BC. CD. D