题目内容
工业上制备纯硅的热化学反应方程式为:SiCl4(g) + 2H2(g) Si(s) + 4HCl(g);△H =" +" Q kJ/mol(Q>0),一定温度、压强下,将一定量的反应物充入密闭容器中进行以上反应,下列叙述正确的是( )
Si(s) + 4HCl(g);△H =" +" Q kJ/mol(Q>0),一定温度、压强下,将一定量的反应物充入密闭容器中进行以上反应,下列叙述正确的是( )
 Si(s) + 4HCl(g);△H =" +" Q kJ/mol(Q>0),一定温度、压强下,将一定量的反应物充入密闭容器中进行以上反应,下列叙述正确的是( )
Si(s) + 4HCl(g);△H =" +" Q kJ/mol(Q>0),一定温度、压强下,将一定量的反应物充入密闭容器中进行以上反应,下列叙述正确的是( )| A.反应过程中,若增大压强能提高硅的产率 |
| B.若反应开始时H2为2 mol,则达到平衡时,吸收热量为Q kJ |
| C.反应至4 min时,若HCl的浓度为0.12 mol/L,则H2的反应速率为0.03 mol/(L·min) |
| D.当反应吸收热量为0.025Q kJ时,生成的HCl通入100 mL 1 mol/L的NaOH溶液中能恰好完全反应 |
D
A项,增大压强,平衡逆向移动,硅的产率降低,A不正确。H2为2 mol,如果完全反应,则吸收热量为Q kJ,该反应是一个可逆反应,所以应小于Q kJ,B不正确。
C项,HCl的反应速率为0.03 mol/(L·min),根据速率比等于化学系数比,知H2的反应速率为0.15 mol/(L·min),所以C项不正确。当反应吸收热量为0.025Q kJ时,说明有0.1mold的HCl生成,所以D正确。
C项,HCl的反应速率为0.03 mol/(L·min),根据速率比等于化学系数比,知H2的反应速率为0.15 mol/(L·min),所以C项不正确。当反应吸收热量为0.025Q kJ时,说明有0.1mold的HCl生成,所以D正确。

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
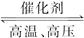 2NH3(g);ΔH=-92.4 kJ·mol-1。
2NH3(g);ΔH=-92.4 kJ·mol-1。

 2C(g),一段时间后达到平衡,生成amolC,则下列说法中正确的是
2C(g),一段时间后达到平衡,生成amolC,则下列说法中正确的是 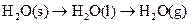
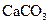 ══
══ 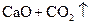
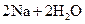 ══
══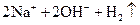
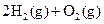 ══
══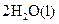
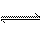 pC(g)+qD(g),生成物C的体积分数与压强p1和p2,时间t1和t2的关系如下图所示,则下列关系正确的是( )
pC(g)+qD(g),生成物C的体积分数与压强p1和p2,时间t1和t2的关系如下图所示,则下列关系正确的是( )
 bB(g)达到平衡后,保持温度不变,将容器体积增加1倍,当达到新平衡时,8的浓度是原来的60%,下列说法正确的是
bB(g)达到平衡后,保持温度不变,将容器体积增加1倍,当达到新平衡时,8的浓度是原来的60%,下列说法正确的是
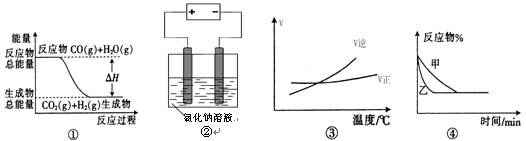

 CO2(g)+H2(g)”中的ΔH大于0
CO2(g)+H2(g)”中的ΔH大于0