题目内容
【题目】某温度下,向一定体积0.1molL﹣1的醋酸溶液中逐滴加人等浓度的NaOH溶液,溶液中 pOH[pOH=﹣lgc(OH﹣)]与 pH 的变化关系如,图所示,则( ) 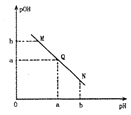
A.M点所示溶液的导电能力强于Q点
B.N点所示溶液中 c(CH3COO﹣)>c(Na+)
C.Q点消耗NaOH溶液的体积等于醋酸溶液的体积
D.M点和N点所示溶液中水的电离程度相同
【答案】D
【解析】解:A.M点主要是醋酸,Q点主要是醋酸钠,由于醋酸是弱酸,电离程度很小,离子浓度也较小,所以M点所示溶液的导电能力弱于Q点,故A错误;
B.N点所示溶液为碱性,则c(OH﹣)>c(H+),根据溶液电荷守恒c(CH3COO﹣)+c(OH﹣)=c(Na+)+c(H+),可判断出此时c(Na+)>c(CH3COO﹣),故B错误;
C.Q点的pOH=pH,溶液为中性,而两者等体积混合后生成醋酸钠,水解显碱性.则所加NaOH溶液体积略小于醋酸溶液的体积,故C错误;
D.由于M点的OH﹣浓度等于N点的H+浓度,对水的电离程度抑制能力相同,所以两点水电离程度相同,故D正确.
故选D.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目